El rápido avance en Medicina Regenerativa e Ingeniería de Tejidos ha impulsado un creciente interés hacia la traslación clínica de tecnologías innovadoras. Sin embargo, el progreso de datos preclínicos prometedores para lograr una autorización exitosa en el mercado clínico sigue siendo un cuello de botella significativo. Uno de los principales obstáculos para avanzar hacia la clínica es la transición de la investigación en animales pequeños a estudios preclínicos avanzados en animales grandes, necesarios para probar la seguridad y eficacia de los productos. Para obtener conclusiones significativas y fiables de los experimentos con animales, es fundamental que la especie y el modelo de enfermedad elegidos sean relevantes para responder tanto a la pregunta de investigación como al problema clínico. La selección del modelo animal más apropiado requiere un conocimiento profundo de especies y razas específicas para asegurar la adecuación del modelo y que las medidas de resultado reflejen fielmente la situación clínica.
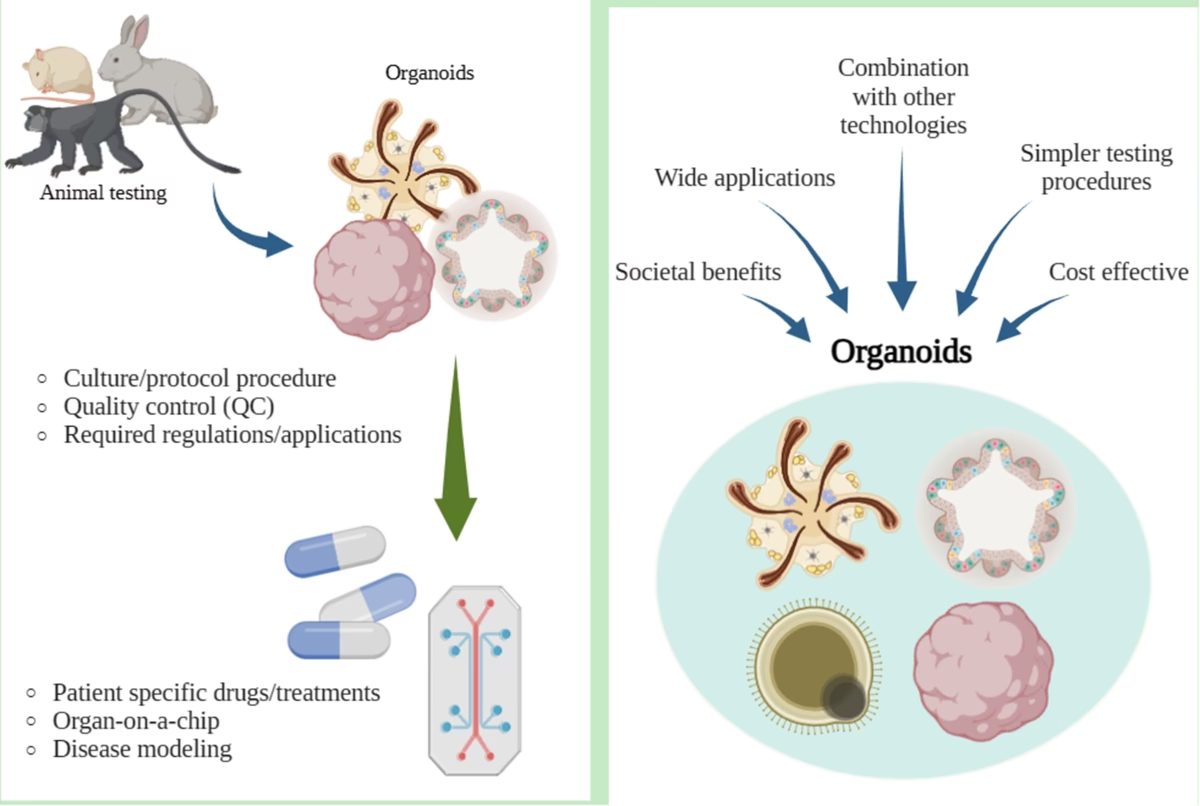
Los enfoques reduccionistas tradicionales en experimentos con animales, que a menudo no reflejan suficientemente la enfermedad estudiada, siguen siendo la norma y pueden resultar en una desconexión entre los resultados observados en estudios con animales y ensayos clínicos. Para abordar estas preocupaciones, se requerirá una reconsideración del enfoque. Esto debería incluir una estrategia por etapas utilizando experimentos in vitro y ex vivo, así como modelos in silico para minimizar la necesidad de estudios in vivo para la detección y el desarrollo temprano, seguidos de modelos de animales grandes que se asemejen más a la enfermedad humana. Las enfermedades que ocurren naturalmente, o espontáneamente, en animales grandes siguen siendo un recurso en gran parte sin explotar y, dadas las similitudes en la fisiopatología con los humanos, no solo permiten estudiar nuevas estrategias de tratamiento, sino también la etiología y prevención de la enfermedad. Los modelos de enfermedades que ocurren naturalmente, particularmente en especies de animales grandes de vida más larga, permiten estudiar trastornos a una edad en la que la enfermedad es más prevalente. Como estas enfermedades suelen ser también una preocupación en la especie veterinaria elegida, se beneficiarían de las terapias recién desarrolladas. Una mayor conciencia del progreso en los modelos animales es mutuamente beneficiosa para los animales, los investigadores, los pacientes humanos y veterinarios.
- El Desafío de la Traslación Clínica
- La Importancia de los Modelos Animales Grandes
- Enfermedades Naturales: Un Recurso Invaluable
- Consideraciones Éticas y las 3 R's
- Tipos Teóricos de Modelos Animales en Investigación
- Modelos Animales Comúnmente Utilizados en Medicina Regenerativa
- Tabla Comparativa: Modelos Animales Pequeños vs. Grandes
- Desafíos y Colaboración Futura
- Preguntas Frecuentes sobre Modelos Animales en Medicina Regenerativa
- Conclusión
El Desafío de la Traslación Clínica
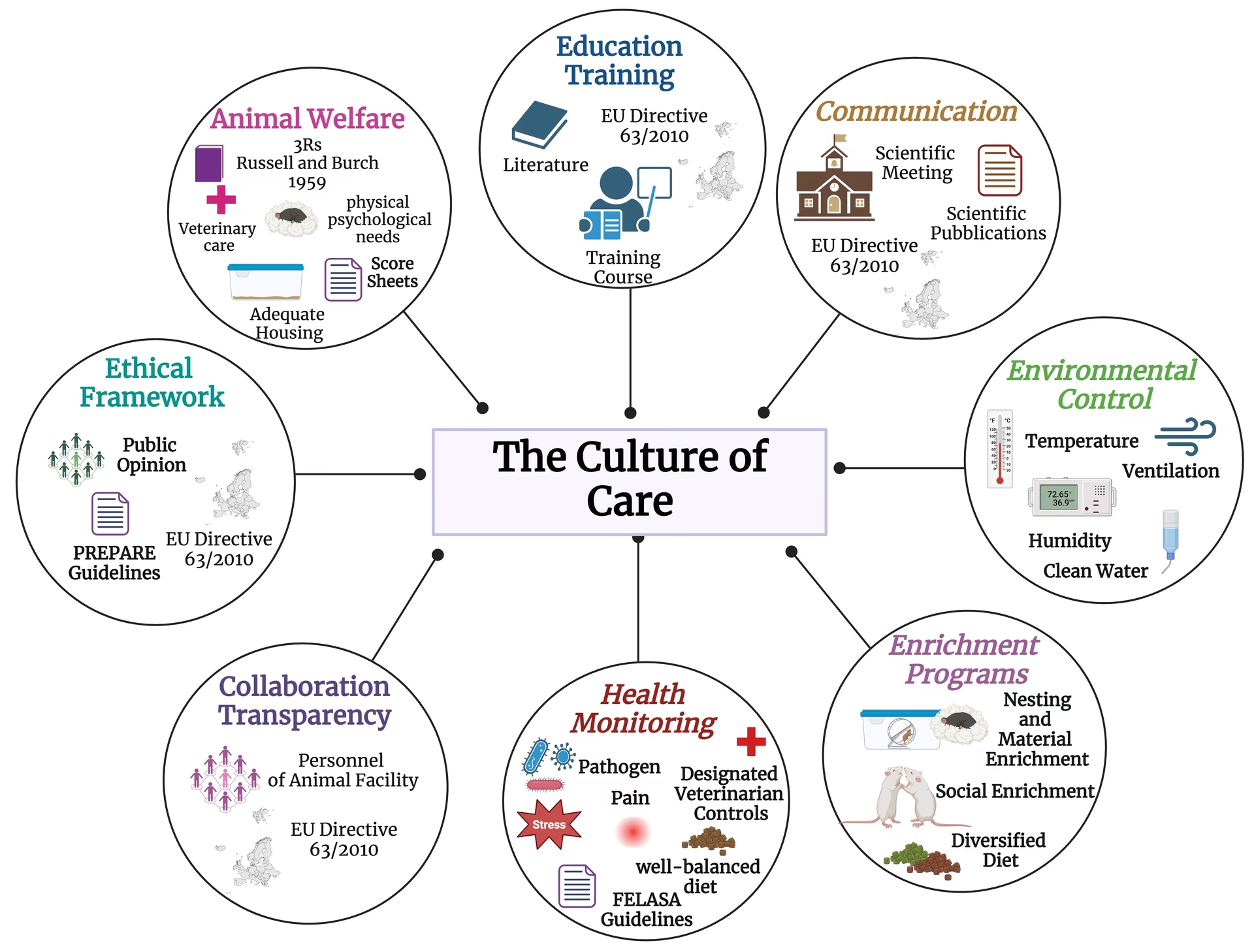
El uso de animales sintientes con fines de investigación es un tema controvertido que ha generado preocupación pública y ética, y es criticado por opositores que afirman que los modelos animales a menudo no generan un beneficio apropiado en relación con sus riesgos y daños potenciales y, como consecuencia, a menudo no son éticamente permisibles. El creciente estatus de las mascotas como miembros de la familia y el correspondiente alto nivel de atención veterinaria para las mascotas privadas amplifican aún más la controversia sobre el uso de animales con fines de investigación.
Sin embargo, los modelos animales siguen siendo un componente importante y, a nivel regulatorio, obligatorio de la investigación traslacional que aún no puede ser reemplazado por experimentos in vitro. Aunque los modelos in vitro permiten un análisis sistemático y estandarizado de diversas señales celulares, biofísicas y bioquímicas en un entorno controlado, sin la variabilidad natural inherente a los modelos animales in vivo, solo pueden ofrecer una visión abstracta de la fisiopatología de las enfermedades y trastornos. Por lo tanto, si bien los modelos animales aún no pueden ser reemplazados, el número de animales utilizados debe reducirse al mínimo y los experimentos que involucran animales deben optimizarse en cuanto a su traslabilidad y el bienestar de los animales.
Hasta la fecha, se emplea comúnmente un enfoque reduccionista que a menudo utiliza especies de laboratorio inmaduras. Los animales roedores pequeños, específicamente ratones y ratas, son valiosos para la investigación de los mecanismos de la enfermedad y la biología fundamental, pero los hallazgos de estos modelos de animales pequeños a menudo no se traducen en aplicaciones clínicas humanas. Shanks et al. ilustraron de manera impresionante los desafíos traslacionales, mostrando la diferencia en la biodisponibilidad de productos farmacéuticos entre humanos, primates, perros y roedores. Sin embargo, aunque la conciencia está aumentando, todavía existe una desproporción masiva entre los estudios con roedores y los estudios con animales grandes.
La Importancia de los Modelos Animales Grandes
Por lo tanto, la Agencia Europea de Medicamentos (EMA), la Administración Federal de Alimentos y Medicamentos de EE. UU. (FDA) y la Sociedad Internacional para la Investigación de Células Madre (ISSCR) recomiendan el uso de modelos de animales grandes para evaluar la eficacia, durabilidad, respuesta a la dosis, degradación y seguridad de los productos medicinales de terapia avanzada (ATMPs). Para una traslación exitosa y oportuna de modelos animales a la aprobación regulatoria y aplicación clínica, sería más apropiado un desarrollo por etapas utilizando animales de laboratorio para la detección y el trabajo de desarrollo temprano, seguido de un modelo de animal grande como el cerdo, la oveja o el caballo, que ofrece un enfoque más realista para el desarrollo tardío y los estudios pivotales.
Enfermedades Naturales: Un Recurso Invaluable
Además, los animales desarrollan muchas enfermedades que ocurren naturalmente (o espontáneamente) que son equivalentes a las enfermedades humanas, lo que lleva al desarrollo del concepto «Una Salud, Una Medicina» (One Health One Medicine), que presupone que las enfermedades en hombres y animales (principalmente mamíferos) tienen etiologías y fisiopatologías similares y requieren enfoques terapéuticos análogos. Por lo tanto, la medicina humana y veterinaria pueden beneficiarse mutuamente de la investigación que aplica un enfoque de una salud. El uso de modelos de animales grandes con enfermedades que ocurren naturalmente con una fisiopatología similar a la de los humanos permite estudiar no solo nuevas estrategias de tratamiento, sino también el desarrollo y la prevención de enfermedades a una edad relevante. Sin embargo, aunque el uso de modelos de enfermedades que ocurren naturalmente refleja mejor la complejidad de la enfermedad, la estandarización del grado de la enfermedad y la disponibilidad de un número suficiente de casos clínicos para la inclusión en los estudios pueden ser desafiantes.
Consideraciones Éticas y las 3 R's
Para lograr el mejor resultado siguiendo el principio de las tres R's (reducir, refinar y reemplazar modelos animales) de usar el menor número posible de animales, los modelos animales deben optimizarse en la mayor medida posible. Requieren una selección y diseño cuidadosos para asegurar que sean adecuados para el propósito y aborden tanto una validez predictiva óptima como consideraciones éticas, de bienestar animal y sociales. Es necesario considerar aspectos de especie, anatómicos, fisiológicos, biomecánicos y su relevancia clínica.
Además, el conocimiento sobre la epidemiología y la historia natural de las enfermedades en diferentes especies animales, las similitudes de las enfermedades con los humanos, la disponibilidad de diagnósticos, opciones de tratamiento y medidas de resultado, así como los criterios que definen la calidad de vida específica de la especie y los parámetros funcionales, es importante pero aún escaso en la comunidad científica. Otras consideraciones importantes al usar modelos de animales grandes incluyen la disponibilidad, el manejo y las preocupaciones económicas.
Para optimizar el resultado científico y el potencial traslacional con las necesidades de bienestar animal, es necesaria una estrecha cooperación entre la ciencia básica, la medicina humana y la veterinaria. El entorno académico veterinario ofrece una experiencia única para lograr ese objetivo con los más altos estándares. Esto incluye el conocimiento veterinario necesario para tomar una decisión racional sobre la elección del modelo animal en lugar de basarse en la disponibilidad interna.
Existen varios grupos de investigación con experiencia en el desarrollo de modelos preclínicos de animales grandes, algunos de los cuales han logrado traducir su investigación en aplicaciones clínicas. Esta lista, de ninguna manera exhaustiva, demuestra claramente los esfuerzos colectivos de la comunidad veterinaria para proporcionar modelos de animales grandes para su uso en proyectos traslacionales.
Sin embargo, todavía se argumenta a menudo que los estudios traslacionales que utilizan modelos de animales grandes son raros porque son complejos, requieren mucho tiempo, son técnicamente exigentes, lentos y generalmente no son adecuados para investigaciones mecanísticas. No obstante, debido a que los animales grandes reflejan mejor la conformación del cuerpo humano y la fisiopatología de ciertas enfermedades que ocurren naturalmente que los modelos con roedores, estos estudios son esenciales, justificando los desafíos y costos. Desafortunadamente, el valor añadido de la relevancia clínica de los modelos de animales grandes a menudo no es apreciado por los revisores de manuscritos y las solicitudes de subvención reciben puntuaciones bajas por falta de conocimiento mecanístico y novedad conceptual insuficiente. Sin embargo, para una traslación exitosa de la investigación en ingeniería de tejidos y medicina regenerativa a terapias clínicas, es fundamental que se corrija esta percepción errónea.
Es la esperanza de los autores que esta revisión, que presenta diferentes modelos de animales grandes, sus enfermedades que ocurren naturalmente y sus especificidades, pueda estimular a los investigadores biomédicos a buscar el mejor modelo posible para su pregunta de investigación específica y que fomente la cooperación interdisciplinaria para optimizar la elección de modelos animales relevantes para la enfermedad en el futuro. Decidir qué modelo animal debe utilizarse en un estudio particular depende, ante todo, de definir la pregunta específica que debe responderse. Solo entonces se pueden considerar los beneficios y desventajas pertinentes de los modelos individuales y tomar una decisión.
En esta revisión, nos centramos en caballos, ovejas, perros, gatos y cerdos como los modelos de animales grandes más utilizados en investigación y no incluimos primates debido a la dimensión ética y las indicaciones limitadas que requieren su uso específico. El uso de animales tan similares a los humanos plantea serias preocupaciones éticas. Por lo tanto, el uso de primates no humanos está estrechamente supervisado y estrictamente regulado, y se ha hecho mucho para salvaguardar específicamente a estos animales. El uso de grandes simios ha sido completamente prohibido. Mientras se utilicen primates no humanos para investigación médica, la Comisión Europea aboga firmemente por el principio de las «3R», ahora una obligación legal incorporada en la legislación de la UE para: Reemplazar primates no humanos con alternativas viables siempre que sea factible, Reducir el uso de primates no humanos y Refinar los procedimientos científicos y el cuidado y tratamiento de los animales. Incluso se discute la eliminación progresiva del uso de primates no humanos en Europa.
Tipos Teóricos de Modelos Animales en Investigación
Aunque existen varias formas diferentes de subdividir los modelos animales, basadas en técnicas, especies o trastornos, una subdivisión más teórica se basa en la pregunta de investigación abordada. Utilizando este enfoque, podemos distinguir entre diferentes clases de modelos animales. Es importante darse cuenta, sin embargo, de que estos modelos a menudo se cruzan y no deben verse como completamente complementarios.
Una definición muy amplia de un modelo animal es «la preparación en una especie con el fin de estudiar fenómenos en otra especie». Según esta definición, probar un nuevo producto veterinario para caballos en una rata o un ratón se consideraría un modelo animal. En el contexto actual (y de hecho, la gran mayoría de los modelos animales descritos en la literatura científica), sin embargo, los modelos animales se desarrollan para estudiar la especie humana. Otra definición utilizada a menudo fue acuñada originalmente por McKinney: «En el caso de los modelos animales para la psicopatología humana, se busca desarrollar síndromes en animales que se asemejen a los de los humanos de ciertas maneras para estudiar aspectos seleccionados de la psicopatología humana». Aunque intuitivamente, esto parece una definición válida y completa, de hecho se limita a un solo grupo específico de modelos animales generalmente denominados modelos de simulación. Sin embargo, también existen otras clases de modelos animales. Una forma útil de subdividir los modelos animales se basa en el objetivo y enfoque principal del modelo. Antes de discutir estos modelos con más detalle, es importante comprender que la subdivisión es algo artificial, y a menudo un modelo animal puede tener múltiples objetivos y, por lo tanto, pertenecer a diferentes clases dependiendo de cómo se utilice.
Las clases principales de modelos, basadas en su objetivo, incluyen:
Modelos de Cribado (Screening Models)
El objetivo principal de los modelos de cribado, a veces denominados pruebas de cribado o modelos con isomorfismo farmacológico, es predecir las propiedades farmacológicas en humanos basándose en sus propiedades en animales. Por lo tanto, el enfoque principal de estos modelos es la farmacoterapia. En su forma más simple, se basan en la premisa de que si dos fármacos producen efectos similares en animales, también producirán efectos similares en humanos. En otras palabras, en estos modelos, un nuevo fármaco se compara con un fármaco bien conocido, generalmente denominado el estándar de oro. Los modelos de cribado han sido muy exitosos en la investigación para el desarrollo de fármacos en los últimos 50 años. De hecho, la gran mayoría de los fármacos en el campo de la terapéutica del SNC se han identificado sobre la base de dichos modelos de cribado.

Sin embargo, existen una serie de limitaciones inherentes a los modelos de cribado. La limitación más importante es que todos los fármacos se comparan con un estándar de oro, y por lo tanto, todos los fármacos serán como el estándar de oro. En otras palabras, tales modelos crean «más de lo mismo» tipo de fármacos. Pueden ser más potentes, tener una duración de acción más prolongada o quizás menos efectos secundarios, pero es poco probable que se identifique un gran avance, como un fármaco con un modo de acción completamente nuevo, en tales modelos. Otra limitación obvia de los modelos de cribado es que es muy difícil desarrollar fármacos para una afección en la que hasta ahora el tratamiento ha sido limitado. Como resultado de estas limitaciones (en combinación con reglas más estrictas de las autoridades reguladoras), los modelos de cribado han perdido su posición destacada en las últimas décadas.
Bioensayos Farmacológicos (Pharmacological Bioassays)
Los bioensayos farmacológicos son la clase de modelos centrados en probar fármacos con un modo de acción bioquímico conocido. Al igual que con los modelos de cribado, el tipo de comportamiento que se utiliza no es esencial e incluso puede ser un cambio fisiológico, como un aumento en la frecuencia cardíaca o un cambio característico en el EEG. Sin embargo, si se desarrolla un fármaco para un trastorno del SNC, es importante que el parámetro de lectura esté relacionado con cambios en el SNC para asegurar que el fármaco sea capaz de cruzar la barrera hematoencefálica.
Bioensayos de Neurociencia (Neuroscience Bioassays)
Esta es una clase muy grande de modelos animales. En estos modelos, la neurobiología es el foco central y el objetivo de estos modelos es identificar el papel de estructuras cerebrales o neurotransmisores específicos en comportamientos u otros procesos fisiológicos. Por lo tanto, estas clases de modelos tendrían como objetivo responder preguntas como: «¿Juega la corteza prefrontal medial un papel en la extinción del miedo?» o «¿Cuál es la implicación del receptor de histamina H3 en el comportamiento exploratorio?». Sin embargo, el parámetro de salida no tiene que ser necesariamente un comportamiento, siempre que sea un parámetro in vivo.
Modelos de Simulación (Simulation Models)
La última clase de modelos animales y, para nuestro propósito actual, la más importante, es la clase de los modelos de simulación. Estos modelos tienen como objetivo imitar el trastorno humano en un animal lo más fielmente posible. También se les ha denominado modelos animales con validez de constructo o modelos con procesos psicológicos entre especies. En la situación más óptima, un modelo de simulación imita la etiología humana, lo que debería conducir a la misma patología y síntomas en los animales. Sin embargo, desarrollar modelos de simulación es una tarea muy difícil, particularmente para los trastornos del SNC, por varias razones. En primer lugar, para la gran mayoría de las enfermedades relacionadas con el SNC, ni la etiología ni la patología son conocidas. Por lo tanto, en el mejor de los casos, solo podemos intentar imitar una etiología hipotética. Además, la mayoría de los síntomas observados en pacientes con trastornos psiquiátricos no son de naturaleza conductual y solo pueden determinarse mediante una entrevista con el paciente. Por lo tanto, dichos síntomas (como, por ejemplo, alucinaciones auditivas o ideación suicida) no pueden determinarse en animales.
Cuando no es posible imitar la etiología o la patología, se puede intentar utilizar un enfoque farmacológico. En este enfoque, se aprovecha el hecho de que existen fármacos específicos que pueden imitar (aspectos de) un trastorno en voluntarios sanos y a menudo exacerban los síntomas existentes en pacientes. Basado en el mismo principio que los modelos de cribado, la idea es que si estos fármacos inducen ciertos (aspectos de) trastornos psiquiátricos en humanos, también lo harán en animales. Aunque en la mayoría de los casos esto es cierto hasta cierto punto, esta categoría de modelos de simulación tiene una debilidad inherente. En humanos, estos fármacos solo inducen efectos agudos de corta duración, mientras que es probable que los trastornos psiquiátricos se desarrollen durante períodos prolongados de tiempo, y por definición, los síntomas deben persistir durante un período de tiempo significativo (semanas a meses).
Cuando todos los enfoques mencionados anteriormente no tienen éxito, aún son posibles algunas alternativas. Dichos modelos generalmente comienzan investigando uno (o más) de los síntomas del trastorno que nos interesa. Un enfoque es comparar diferentes cepas de ratas o ratones para investigar si alguna de ellas muestra «espontáneamente» este síntoma. Alternativamente, se pueden buscar síntomas que ocurren espontáneamente dentro de una cepa y, asumiendo que esto ocurra, criar selectivamente estos animales que exhiben síntomas para producir líneas de selección.
Modelos Animales Comúnmente Utilizados en Medicina Regenerativa
Si bien el texto proporciona una clasificación teórica de los modelos animales en general, al hablar de Medicina Regenerativa y la traslación clínica, la relevancia de las especies específicas y la presencia de enfermedades naturales cobra particular importancia. Los animales grandes son preferidos en las etapas avanzadas de desarrollo preclínico debido a su tamaño, fisiología y similitud con los humanos en ciertas patologías. Las especies frecuentemente mencionadas y utilizadas en este campo incluyen:
- Caballos
- Ovejas
- Perros
- Gatos
- Cerdos
El valor de estas especies radica en que desarrollan muchas enfermedades que reflejan afecciones humanas, permitiendo estudiar terapias regenerativas en un contexto más realista que los modelos con roedores.
Tabla Comparativa: Modelos Animales Pequeños vs. Grandes
Para ilustrar las diferencias clave que influyen en su uso en la investigación traslacional en medicina regenerativa, podemos comparar las características generales de los modelos animales pequeños (como roedores) y grandes:
| Criterio | Animales Pequeños (Roedores) | Animales Grandes (Cerdos, Caballos, etc.) |
|---|---|---|
| Tamaño/Fisiología | Significativamente diferente a humanos. | Más similar a humanos en tamaño y algunos aspectos fisiológicos. |
| Traslación Clínica | Hallazgos a menudo no se traducen bien a humanos. | Mejor predictibilidad para aplicaciones clínicas humanas. |
| Costo/Manejo | Generalmente menor costo y más fácil manejo. | Mayor costo y manejo más complejo. |
| Enfermedades Naturales | Menos comunes o relevantes para enfermedades humanas complejas. | Desarrollan muchas enfermedades espontáneas similares a las humanas. |
| Estudios Mecanísticos | Excelentes para estudios de mecanismos básicos. | Menos adecuados para estudios mecanísticos a gran escala, más para eficacia y seguridad. |
| Estudios de Eficacia/Seguridad ATMPs | Menos recomendados por agencias regulatorias. | Recomendados por agencias regulatorias (EMA, FDA) para etapas avanzadas. |
| Consideraciones Éticas | Preocupaciones éticas presentes. | Preocupaciones éticas a menudo amplificadas (ej. mascotas, tamaño). |
Desafíos y Colaboración Futura
A pesar de sus ventajas para la traslación, los modelos con animales grandes enfrentan desafíos. Son complejos, requieren mucho tiempo y son técnicamente exigentes. La estandarización de las enfermedades naturales y la disponibilidad de suficientes casos clínicos pueden ser obstáculos. Además, a menudo no son tan adecuados como los roedores para estudios mecanísticos detallados, lo que a veces lleva a que su valor sea subestimado por los revisores que priorizan la investigación básica sobre la relevancia clínica.
Para superar estos desafíos y optimizar la investigación traslacional, es fundamental una estrecha colaboración interdisciplinaria entre la ciencia básica, la medicina humana y la medicina veterinaria. Los veterinarios académicos, en particular, poseen un conocimiento crucial sobre las enfermedades en diferentes especies animales y la experiencia necesaria para seleccionar y utilizar el modelo más apropiado para una pregunta de investigación específica.
Preguntas Frecuentes sobre Modelos Animales en Medicina Regenerativa
Q: ¿Por qué son necesarios los modelos animales en la investigación en medicina regenerativa?
A: Son esenciales y, a menudo, requeridos por las agencias regulatorias para evaluar la seguridad y eficacia de nuevas terapias en un organismo vivo y complejo antes de pasar a ensayos en humanos. Permiten estudiar cómo interactúan las terapias con diferentes tejidos, sistemas y el entorno inmunológico de una manera que los modelos in vitro no pueden replicar.
Q: ¿Qué ventajas ofrecen los animales grandes sobre los roedores para la traslación clínica en este campo?
A: Los animales grandes tienen un tamaño y fisiología más parecidos a los humanos, lo que es crucial para evaluar la entrega, distribución y funcionalidad de biomateriales o células diseñadas para aplicaciones clínicas. Además, a menudo desarrollan enfermedades espontáneas que imitan de cerca las condiciones humanas, proporcionando un modelo más relevante para probar terapias regenerativas.
Q: ¿Qué significa utilizar enfermedades que ocurren naturalmente como modelos?
A: Significa estudiar enfermedades que los animales desarrollan por sí solos, en lugar de inducirlas experimentalmente. Estos modelos son valiosos porque la enfermedad se desarrolla de manera más similar a cómo lo haría en humanos, a menudo a una edad comparable, lo que mejora la relevancia traslacional de los estudios.
Q: ¿Cuáles son las principales preocupaciones éticas y cómo se abordan?
A: Las principales preocupaciones giran en torno al bienestar animal y la justificación del uso de animales sintientes. Se abordan mediante la aplicación estricta del principio de las 3 R's: Reducir el número de animales, Refinar los procedimientos para minimizar el sufrimiento y Reemplazar los animales por alternativas siempre que sea posible.
Q: ¿Qué especies de animales grandes son comúnmente utilizadas en medicina regenerativa?
A: Especies como caballos, ovejas, perros, gatos y cerdos son frecuentemente utilizadas debido a su relevancia para modelar diversas afecciones que podrían beneficiarse de terapias regenerativas, ya sea por su tamaño, fisiología o la presencia de enfermedades naturales relevantes.
Conclusión
La selección adecuada del modelo animal es un factor crítico para el éxito de la traslación de la investigación en medicina regenerativa desde el laboratorio a la clínica. Si bien los modelos con roedores son valiosos para estudios básicos, la necesidad de modelos de animales grandes que reflejen más fielmente la complejidad de las enfermedades humanas y permitan la evaluación de la seguridad y eficacia de las terapias en un contexto clínicamente relevante es innegable. El uso de enfermedades que ocurren naturalmente en animales grandes ofrece una oportunidad única para estudiar la enfermedad y probar tratamientos en un entorno más predictivo. Superar los desafíos logísticos, técnicos y de percepción asociados con estos modelos requiere una colaboración más estrecha entre las diversas disciplinas de investigación. Al elegir cuidadosamente el modelo animal más adecuado para cada pregunta de investigación específica, podemos maximizar el potencial traslacional de la medicina regenerativa, beneficiando tanto a los pacientes humanos como a los animales.
Si quieres conocer otros artículos parecidos a Modelos Animales en Medicina Regenerativa puedes visitar la categoría Investigación.