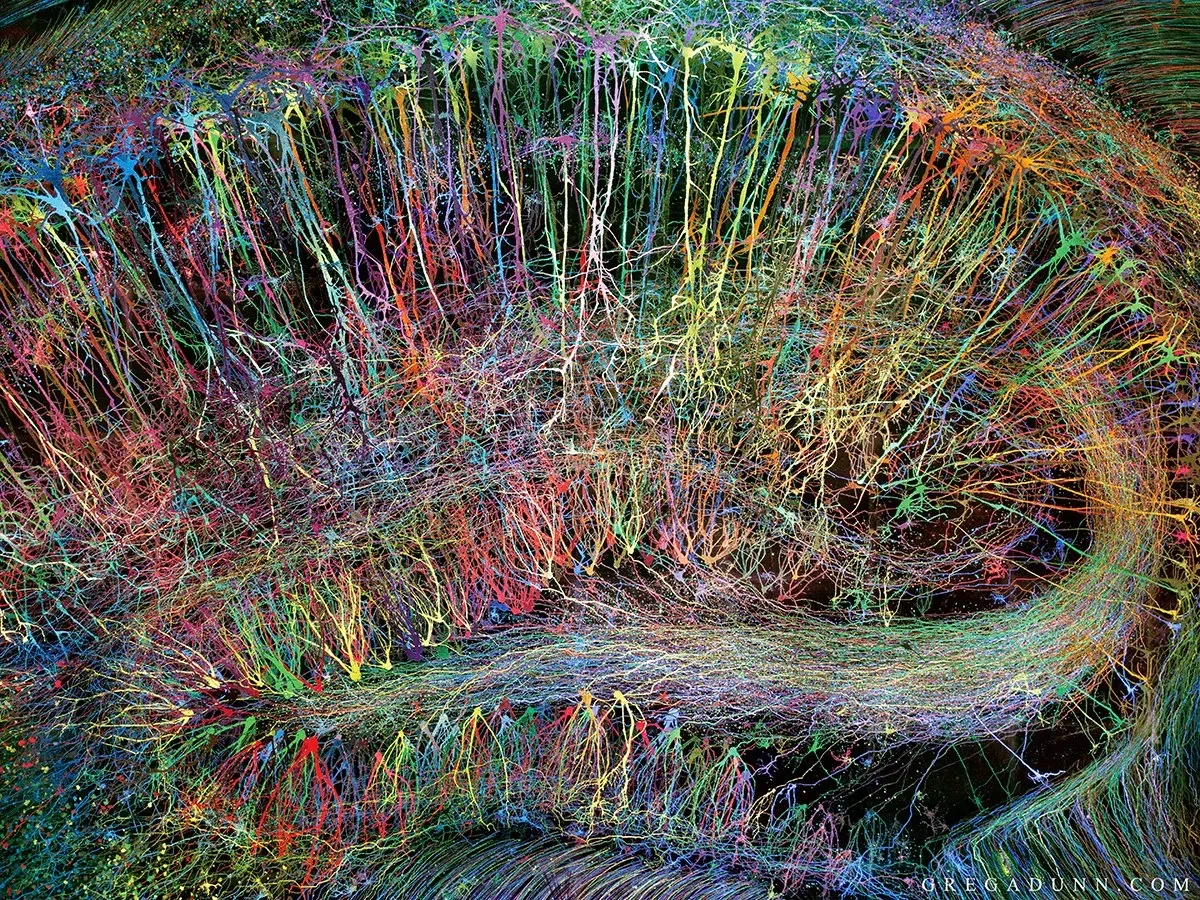
La neurociencia moderna busca comprender la intrincada red de células que componen el sistema nervioso. Visualizar la arquitectura y las conexiones entre neuronas y células gliales es fundamental, pero la complejidad de estos tejidos presenta un desafío enorme. Aquí es donde técnicas innovadoras como Brainbow han revolucionado el campo, permitiendo a los científicos 'pintar' células individuales con una variedad de colores distintivos.

Brainbow es una estrategia de marcaje multicolor que utiliza la recombinación Cre-lox para expresar de forma estocástica (aleatoria) entre dos y cuatro proteínas fluorescentes (FP) en las células de un tejido. La combinación específica de FP expresada en cada célula depende del número de copias de los sitios loxP presentes y de los eventos de recombinación que ocurran. Esta expresión combinatoria da como resultado una miríada de colores y tonalidades únicas para cada célula, haciendo posible distinguir visualmente neuronas individuales dentro de la densa y compleja organización del tejido nervioso. Inicialmente concebida para el cerebro, esta técnica se ha adaptado y aplicado en diversos organismos y tejidos.
El Principio Detrás del Arcoíris Celular
El fundamento de Brainbow reside en la recombinación genética mediada por la enzima Cre. Los constructos de ADN de Brainbow contienen secuencias que codifican diferentes proteínas fluorescentes, flanqueadas por sitios loxP de distintas especificidades. Cuando la enzima Cre se expresa en una célula, puede inducir la recombinación entre pares de sitios loxP compatibles. Dependiendo de qué pares de sitios loxP recombinen y en qué orden, el ADN se reconfigura, llevando a la expresión de una combinación única de proteínas fluorescentes. Por ejemplo, si se tienen genes para proteínas fluorescentes roja, verde y azul, una célula podría expresar solo la roja, otra la verde y azul, otra las tres, etc., generando así una amplia gama de colores al mezclarse sus emisiones.
Esta diversidad cromática permite a los investigadores rastrear la forma de las neuronas individuales, sus axones y dendritas, e incluso estudiar sus interacciones con células vecinas. Antes de Brainbow, mapear circuitos neuronales complejos a menudo requería inyecciones individuales de colorantes, un proceso laborioso y limitado en la cantidad de células que podían etiquetarse simultáneamente.
Evolución de las Herramientas Brainbow: Hacia UFObow
Aunque las estrategias originales de Brainbow (Brainbow-1 y Brainbow-2) fueron pioneras, las limitaciones en las propiedades de las proteínas fluorescentes y los requisitos de imagen (a menudo necesitando múltiples longitudes de onda de excitación) impulsaron el desarrollo de variantes mejoradas. El texto proporcionado detalla la creación de una nueva herramienta de marcaje multicolor llamada UFObow, diseñada para superar algunas de estas limitaciones, especialmente para la imagen rápida y a gran escala.
El desarrollo de UFObow se centró en la creación de nuevas proteínas fluorescentes excitables por una única longitud de onda (luz azul, alrededor de 405 nm) y con grandes desplazamientos de Stokes (LSS - Large Stokes Shift), lo que minimiza la superposición espectral (bleed-through) y facilita la detección en canales de emisión separados. Se realizaron mutagénesis guiadas por estructura en proteínas fluorescentes ya existentes: mTFP, mKOk y Crimson.
Se desarrollaron tres nuevas proteínas fluorescentes excitables por luz azul:
- mTFP2b: Derivada de mTFP, se realizó una mutación (T63N) para hacerla más tenue y con un desplazamiento hacia el azul en la emisión, reduciendo la superposición con canales de emisión más largos. Su pico de excitación es 459 nm y el de emisión 488 nm.
- LSSmKOb: Desarrollada a partir de mKOk. Se introdujeron mutaciones (como V158D) para inducir la transferencia de protones en estado excitado (ESPT), crucial para el gran desplazamiento de Stokes. Después de múltiples rondas de optimización, se obtuvo una variante brillante excitable por luz azul con picos de excitación en 437 nm (principal) y 550 nm, y emisión en 566 nm.
- LSSfRFP: Creada a partir de Crimson, también incorporando mutaciones para LSS (como C158D). Para desplazar aún más la emisión hacia el rojo, se fusionó en tándem con la proteína dCardinal (una proteína far-red). Después de optimizaciones en el linker entre ellas, se obtuvo LSSfRFP con picos de excitación en 452 nm (LSSCrimson) y 601 nm (dCardinal), y emisión en 637 nm.
Estas nuevas FP (mTFP2b, LSSmKOb, LSSfRFP) fueron caracterizadas por su maduración rápida, baja agregación y fotostabilidad relativa en células vivas. Aunque LSSmKOb y LSSfRFP mostraron cierta superposición espectral, se determinó que la corrección de esta superposición no siempre es necesaria para el análisis de clusters de color, aunque sí es importante para estudios de rastreo de linajes.
La construcción de UFObow reemplazó las FP originales de un diseño previo (Brainbow3.2) con mTFP2b, LSSmKOb y LSSfRFP. Además, se sustituyó una proteína no fluorescente por una luciferasa secretada (secNluc) para evaluar la expresión en ausencia de recombinación de forma sencilla mediante bioluminiscencia. Se utilizó un promotor universal (CAG) en lugar de uno específico de tejido para permitir una expresión más amplia. El nombre UFObow proviene de 'Universal expression', 'Fast acquisition' (debido a la excitación con una sola longitud de onda) y 'Modular design'.
Caracterización de UFObow en Células
Se evaluó sistemáticamente la eficiencia de recombinación, la aleatoriedad de la recombinación y la complejidad del color de UFObow en líneas celulares que co-expresaban UFObow y Cre. La eficiencia de recombinación se determinó midiendo la señal de bioluminiscencia de secNluc: una señal baja indicaba una alta recombinación. Se encontró una eficiencia superior al 94%.
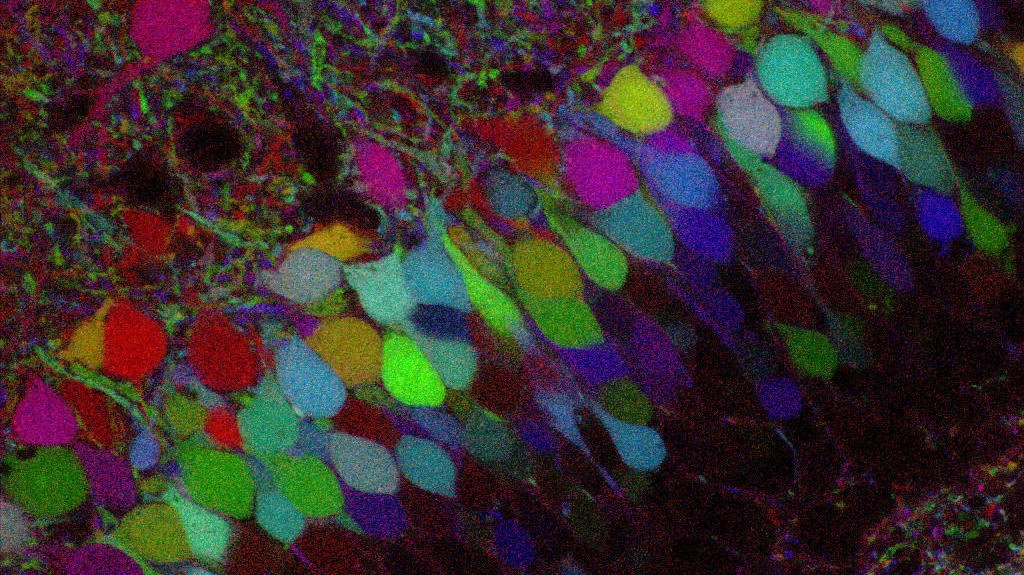
La aleatoriedad se evaluó contando el número de células que expresaban cada una de las tres FP; se observó una distribución comparable, indicando que Cre actuaba de manera equivalente en cada par de sitios lox.
La complejidad del color se analizó utilizando el algoritmo K-means en el espacio de color Hue-Saturation (HS). Se identificaron múltiples clusters de color distintos (63 en células HeLa, 69 en células B16), demostrando la capacidad de UFObow para marcar células con una rica variedad de colores.
Aplicaciones de UFObow en Vivo
UFObow ha demostrado ser una herramienta poderosa para diversas aplicaciones en organismos vivos, particularmente ratones transgénicos:
Marcaje Específico de Tipos Celulares
Cruzando ratones transgénicos UFObow con ratones Cre específicos de tipo celular, se logró etiquetar poblaciones celulares específicas en diferentes órganos. Por ejemplo, se generaron ratones CX3CR1cre:UFObow (para macrófagos y células dendríticas), CD11ccre:UFObow (para células dendríticas CD11c+) y Chatcre:UFObow (para neuronas colinérgicas).
Mediante microscopía confocal e inmunofluorescencia, se confirmó la especificidad del marcaje en tejidos como el cerebro, ganglios linfáticos y bazo. Las células que expresaban UFObow colocalizaban con los marcadores específicos de cada tipo celular. La complejidad de color observada en estos tejidos (entre 40 y 60 colores distintos) permitió diferenciar numerosas células dentro de estas poblaciones específicas.
Mapeo Rápido de la Distribución Celular en Grandes Volúmenes
Una ventaja significativa de UFObow es su excitación con una sola longitud de onda, lo que acelera enormemente los procesos de imagen en comparación con las técnicas convencionales que requieren escaneo secuencial con múltiples láseres. Esto es crucial para mapear la distribución espacial tridimensional de células en tejidos de varios milímetros cúbicos con resolución de célula individual.
Se utilizó UFObow para mapear macrófagos y vasos sanguíneos en el hígado de un ratón CX3CR1cre:UFObow. Mediante una técnica de microscopía de sección óptica por criofluorescencia, se obtuvieron miles de imágenes de alta resolución de un lóbulo hepático completo. La excitación con una sola longitud de onda permitió una adquisición de datos mucho más rápida. La reconstrucción 3D reveló la distribución espacial de los macrófagos en relación con las venas hepáticas y portales. El análisis cuantitativo mostró que los macrófagos se enriquecían alrededor de la tríada portal, sugiriendo heterogeneidad en su densidad dentro del lobulillo hepático.
Estudio de la Heterogeneidad de Metástasis Tumorales
La heterogeneidad tumoral es clave en el crecimiento y la metástasis del cáncer. UFObow se utilizó para rastrear la dinámica de crecimiento de clones tumorales en un modelo de metástasis hepática de células B16 de melanoma.
Se generó una línea celular B16 estable que expresaba UFObow y Cre, resultando en células B16 marcadas con múltiples colores (45 colores distintos). Estas células mantuvieron su color después de la división, permitiendo rastrear linajes clonales. Se inyectaron estas células en el bazo de ratones para inducir metástasis hepáticas, y se monitoreó su crecimiento a lo largo del tiempo mediante imagen intravital.
Se observó que en las etapas tempranas y medias, las metástasis eran predominantemente monoclonales, con diferentes clones mostrando distintas dinámicas de crecimiento (creciendo, desapareciendo, o disminuyendo y luego creciendo). En etapas tardías, las metástasis mostraron una mezcla de patrones de crecimiento, con algunos focos de color único y otros con múltiples colores, indicando invasión intratumoral y mezcla clonal.

Además, UFObow permitió visualizar la interacción de los clones tumorales con el microambiente tumoral (TME), como células inmunes y vasos sanguíneos, al combinar el marcaje de UFObow con otros colorantes o FP.
Comparación entre Brainbow Convencional y UFObow
Aunque ambas técnicas se basan en el marcaje multicolor mediante recombinación, UFObow presenta ventajas específicas:
| Característica | Brainbow Convencional (Ej. Brainbow3.2) | UFObow |
|---|---|---|
| Proteínas Fluorescentes | mOrange2, EGFP, mKate2 (requieren excitación con múltiples longitudes de onda) | mTFP2b, LSSmKOb, LSSfRFP (excitables principalmente por luz azul ~405nm) |
| Excitation | Múltiples longitudes de onda | Principalmente una única longitud de onda (~405nm) |
| Velocidad de Imagen | Más lenta (escaneo secuencial por canal) | Más rápida (adquisición simultánea) |
| Evaluación de No-Recombinación | Proteína no fluorescente (requiere inmunofluorescencia) | Luciferasa secretada (secNluc, detectable por bioluminiscencia) |
| Promotor | A menudo específico de tejido (ej. Thy1) | Universal (CAG) |
| Aplicaciones | Mapeo de circuitos neuronales, rastreo de linajes | Mapeo rápido a gran escala, estudio de heterogeneidad, rastreo de linajes, marcaje específico |
Preguntas Frecuentes sobre Brainbow y UFObow
¿Qué es la técnica Brainbow?
Es una técnica de biología molecular que utiliza la recombinación genética mediada por la enzima Cre para generar una amplia gama de colores fluorescentes distintivos en células individuales dentro de un tejido. Esto permite visualizar y diferenciar células vecinas que de otro modo serían indistinguibles.
¿Cómo crea Brainbow múltiples colores en las células?
Brainbow utiliza constructos de ADN con genes de proteínas fluorescentes de diferentes colores (como azul, cian, verde, amarillo, naranja, rojo) flanqueados por secuencias loxP. La enzima Cre induce la recombinación entre estos sitios, llevando a la expresión aleatoria y combinatoria de las FP, lo que resulta en una mezcla de colores única para cada célula.
¿Qué es UFObow y cuáles son sus ventajas?
UFObow es una versión mejorada de Brainbow que utiliza proteínas fluorescentes excitables por una única longitud de onda (luz azul). Sus ventajas incluyen una adquisición de imágenes más rápida, una evaluación sencilla de la recombinación mediante bioluminiscencia y la capacidad de usar un promotor universal para marcar células en diversos tejidos.
¿Para qué se utiliza Brainbow/UFObow en neurociencia?
Se utiliza para mapear la compleja arquitectura de las neuronas y células gliales, rastrear sus proyecciones (axones y dendritas), estudiar la organización de los circuitos neuronales y realizar análisis de rastreo de linajes celulares.
¿Se puede usar Brainbow/UFObow en tejidos vivos?
Sí, ambas técnicas están diseñadas para ser utilizadas en organismos vivos (como ratones transgénicos o moscas Drosophila) para estudios in vivo, permitiendo el seguimiento de células y estructuras a lo largo del tiempo.
¿Qué otros campos además de la neurociencia se benefician de Brainbow?
Aunque nació para el cerebro, Brainbow y sus variantes se aplican en cualquier campo que requiera el marcaje multicolor de células para estudiar su distribución, linaje, interacción o heterogeneidad, como la inmunología, el estudio del cáncer y la biología del desarrollo.
Conclusión
Desde su concepción, la técnica Brainbow ha transformado la forma en que los científicos visualizan y estudian las células dentro de tejidos complejos. La capacidad de 'pintar' células individuales con colores únicos ha abierto nuevas vías para mapear circuitos neuronales, rastrear el destino celular y comprender la organización espacial y la heterogeneidad dentro de órganos. La evolución de esta técnica, ejemplificada por el desarrollo de UFObow con sus proteínas fluorescentes optimizadas y su capacidad para la imagen rápida con una sola longitud de onda, amplía aún más sus aplicaciones, permitiendo estudios a gran escala y con mayor eficiencia. Brainbow y sus sucesores continúan siendo herramientas indispensables en la investigación biomédica, desentrañando la complejidad de los sistemas vivos con una claridad sin precedentes.
Si quieres conocer otros artículos parecidos a Brainbow: Coloreando el Cerebro y Más Allá puedes visitar la categoría Neurociencia.