Más allá de las neuronas y células gliales que conforman la densa red del cerebro, existe un microambiente crucial y a menudo pasado por alto: el espacio extracelular. Este espacio, que rodea cada célula del sistema nervioso central, no es un simple vacío, sino un entorno dinámico lleno de líquido y moléculas, esencial para una multitud de funciones cerebrales. A pesar de su importancia, su estudio ha sido un desafío constante para los neurocientíficos, un territorio que, como las profundidades del espacio, sigue revelando sus secretos gradualmente.
El espacio extracelular (ECS) del cerebro puede definirse como el estrecho entorno que rodea a cada célula del sistema nervioso central, situado fuera de las membranas plasmáticas. Este espacio está ocupado principalmente por un líquido intersticial cuya composición es notablemente similar a la del líquido cefalorraquídeo (LCR), con el añadido de moléculas que conforman la matriz extracelular. Es un componente fundamental que ocupa una fracción significativa del volumen cerebral y desempeña roles vitales en la comunicación, el transporte y el mantenimiento del delicado equilibrio químico y eléctrico del tejido nervioso.
- Composición y Estructura del Espacio Extracelular Cerebral
- Funciones Vitales del ECS para el Cerebro
- Desafíos en la Visualización y Métodos de Medición
- Factores que Afectan la Difusión en el ECS
- Flujo de Líquido Intersticial y la Hipótesis Glifática
- Preguntas Frecuentes sobre el Espacio Extracelular Cerebral
Composición y Estructura del Espacio Extracelular Cerebral
El ECS comprende los espacios llenos de líquido externos a las membranas celulares. Aunque en un sentido amplio podría incluir los vasos sanguíneos, los espacios perivasculares, ventriculares y subaracnoideos, comúnmente se equipara con el espacio intersticial, es decir, los espacios estrechos entre las células del parénquima cerebral. Este líquido intersticial está en comunicación con el LCR en los espacios ventriculares y subaracnoideos.
Un componente esencial del ECS es la matriz extracelular (MEC). La MEC cerebral está compuesta por proteoglicanos, hialuronano (HA) y diversas proteínas de enlace pequeñas. Los proteoglicanos, como los lecticanos (agrecan, versican, neurocan y brevican), tienen un esqueleto proteico del que se extienden cadenas de glicosaminoglicanos (GAGs), formando proteoglicanos de heparán sulfato (HSPGs) o proteoglicanos de condroitín sulfato (CSPGs). Estos últimos, junto con la tenascina-R y el HA, forman importantes estructuras de la MEC, como las llamadas "redes perineuronales" que rodean a ciertas neuronas. Los grupos sulfato en los CSPGs y HSPGs les confieren numerosas cargas negativas.
La estructura física del ECS es notablemente estrecha, con anchos estimados en decenas de nanómetros. A pesar de su estrechez, el ECS es un espacio altamente conectado, descrito a menudo como la "fase acuosa de una espuma", donde cada elemento está vinculado a través de múltiples vías. La fracción de volumen que ocupa el ECS dentro del tejido cerebral es considerable, representando aproximadamente el 20% del total en el cerebro adulto. Sin embargo, este volumen puede variar significativamente en diferentes condiciones, como veremos más adelante.
Funciones Vitales del ECS para el Cerebro
El ECS no es solo un espacio físico; es un entorno funcionalmente activo con múltiples roles:
- Reservorio Iónico: Actúa como un depósito de iones esenciales para la actividad eléctrica neuronal. Iones como el K+ y el Ca2+ se encuentran en el ECS y sus concentraciones pueden fluctuar localmente, afectando el potencial de membrana y la liberación de neurotransmisores.
- Comunicación Química Intercelular: El ECS sirve como un canal para la comunicación química entre células. Más allá de la sinapsis directa, las moléculas señalizadoras pueden difundir a través del ECS para alcanzar receptores en células vecinas o distantes.
- Transmisión de Volumen: También conocida como transmisión extrasináptica, parasináptica, difusa o paracrina, implica la propagación de señales iónicas o moleculares a través del ECS. Neurotransmisores como el glutamato y la dopamina pueden escapar de la hendidura sináptica (spillover) y activar receptores extrasinápticos. También existe evidencia de señalización neurona-glía a través del ECS utilizando sustancias como el glutamato y el ATP.
- Conducción de Volumen: Las propiedades resistivas del ECS contribuyen a la formación de potenciales de campo locales, un componente esencial de la actividad eléctrica cerebral.
Desafíos en la Visualización y Métodos de Medición
La naturaleza estrecha del ECS ha presentado un desafío significativo para su visualización directa. Los intentos de revelar su tamaño y estructura utilizando microscopía electrónica convencional han tenido un éxito limitado, ya que muchos procedimientos de fijación química tienden a colapsar los espacios intercelulares. Técnicas especializadas como la criofijación han demostrado que el ECS puede preservarse y que su ancho puede variar localmente.
Dada la dificultad de la visualización directa, se han desarrollado enfoques biofísicos basados en la difusión de moléculas sonda para estudiar el ECS en tejido vivo y en tiempo real. Estos métodos tratan el cerebro como un medio poroso y cuantifican dos parámetros clave:
- Fracción de Volumen (α): La proporción del tejido cerebral ocupada por el ECS. Se define como α = VECS / VTejido.
- Tortuosidad (λ): Una medida de la resistencia a la difusión que experimentan las moléculas al atravesar la geometría compleja del ECS. Se define como λ = D / D*, donde D es el coeficiente de difusión en solución libre y D* es el coeficiente de difusión efectivo en el tejido. Una tortuosidad de 1.6, por ejemplo, significa que una molécula pequeña tiene un coeficiente de difusión efectivo que es solo dos quintos del que tendría en un medio sin restricciones.
Históricamente, se utilizaron métodos de radiotrazadores, perfundiendo los ventrículos o el espacio subaracnoideo con moléculas como inulina o sacarosa marcadas. Midendo los perfiles de radiactividad en el tejido después de la fijación, se podían estimar α y λ. Sin embargo, esta técnica tenía limitaciones en resolución espacial y temporal.

Extracellular space refers to the part of a multicellular organism outside the cells, usually taken to be outside the plasma membranes, and occupied by fluid. This is distinguished from intracellular space, which is inside the cells. Un avance significativo fue la introducción del método de ioniotoforesis en tiempo real (RTI), basado en el paradigma de fuente puntual. Esta técnica utiliza micropipetas para liberar una pequeña cantidad de una molécula sonda cargada (comúnmente tetrametilamonio, TMA+) mediante una corriente constante, y microelectrodos selectivos de iones para medir la concentración resultante a una distancia conocida. Al analizar la curva de concentración en función del tiempo, se pueden determinar tanto α como λ. El método RTI ha establecido que en la mayoría del tejido cerebral adulto, α es aproximadamente 0.2 (20%) y λ es típicamente 1.6.
El método de imagenología óptica integrativa (IOI) extiende el paradigma de fuente puntual utilizando macromoléculas marcadas con fluoróforos. Al inyectar estas moléculas (como dextranos o proteínas) y seguir su propagación mediante microscopía de epifluorescencia o dos fotones, se puede obtener D* y, por lo tanto, λ. Aunque el IOI no proporciona α directamente, ha sido crucial para investigar cómo la difusión se ve obstaculizada por el tamaño molecular. Estudios con dextranos y puntos cuánticos de hasta 35 nm de diámetro sugieren que el ancho típico de los espacios del ECS es de aproximadamente 40 nm, aunque pueden existir expansiones locales más amplias (microdominios de espacio muerto).
Métodos emergentes, como el seguimiento de nanotubos de carbono de pared simple o la imagenología de anisotropía de fluorescencia resuelta en el tiempo, están comenzando a proporcionar información a escala nanométrica sobre la viscosidad local y las variaciones de ancho en el ECS, complementando los hallazgos de RTI e IOI.
Factores que Afectan la Difusión en el ECS
La tortuosidad (λ) es un parámetro compuesto influenciado por varios factores. Las simulaciones de Monte Carlo sugieren que la geometría básica de un empaquetamiento celular regular generaría una tortuosidad menor (λ ≤ 1.225) que la observada experimentalmente (~1.6). Esto implica la existencia de factores adicionales que obstaculizan la difusión. Uno de estos factores son los microdominios de espacio muerto, que pueden ser invaginaciones celulares, envolturas gliales o expansiones locales del ECS, donde las moléculas pueden quedar transitoriamente atrapadas, aumentando el tiempo efectivo para recorrer una distancia.
La matriz extracelular también juega un papel importante en la modulación de la difusión. Las cargas negativas en los GAGs de los proteoglicanos pueden interactuar con iones cargados. Por ejemplo, la difusión de Ca2+ se ve afectada por la unión reversible a los grupos sulfato de condroitín sulfato, lo que disminuye su coeficiente de difusión efectivo. En contraste, la difusión de iones monovalentes como el TMA+ no se ve afectada significativamente por la eliminación de estos grupos sulfato. Además, moléculas como la lactoferrina pueden unirse reversiblemente a los grupos heparán sulfato de los HSPGs, lo que también reduce su difusión efectiva. Estas interacciones pueden modelarse como un proceso de unión reversible en equilibrio que reduce D* según la fórmula Dm* = D* / (R + 1), donde R está relacionado con la afinidad de unión.
Además de la geometría y la interacción con la MEC, otros factores pueden alterar las propiedades del ECS, incluyendo cambios osmóticos, edema, isquemia y condiciones patológicas como tumores cerebrales.

The two central extracellular compartments of brain are the cerebrospinal fluid (CSF) and the brain interstitial fluid (ISF). The CSF is segregated from the blood by the choroid plexus or blood–CSF barrier and the ISF is segregated from blood by the brain capillary or BBB. Flujo de Líquido Intersticial y la Hipótesis Glifática
Si bien la difusión es el mecanismo dominante para el transporte de sustancias en el ECS en distancias cortas y escalas de tiempo breves, ha habido un debate de larga data sobre si también existe transporte por flujo masivo de líquido intersticial (bulk flow) en distancias más largas y escalas de tiempo mayores.
El líquido intersticial (ISF) y el LCR se secretan continuamente. El ISF se secreta principalmente en el endotelio de la barrera hematoencefálica (BBB), impulsado por la actividad de la Na+/K+-ATPasa. El LCR se secreta en los plexos coroideos. El ISF fluye lentamente a través del tortuoso espacio extracelular del parénquima cerebral y drena hacia el LCR ventricular a través del epéndimo o hacia el LCR subaracnoideo a través de la piamadre. El LCR, a su vez, drena hacia la sangre venosa a través de las granulaciones aracnoideas.
Este flujo y recambio constante de los fluidos extracelulares genera un "efecto sumidero", que ayuda a eliminar solutos del cerebro, incluyendo drogas. La producción de ISF en el parénquima es de aproximadamente 0.17 μl/g de tejido/min, lo que implica un tiempo de recambio del volumen de ISF de aproximadamente 19-20 horas, independientemente del tamaño cerebral. En cerebros más grandes (como el humano), la contribución del ISF a la producción total de líquido extracelular cerebral es proporcionalmente mayor que en cerebros pequeños (como el de rata).
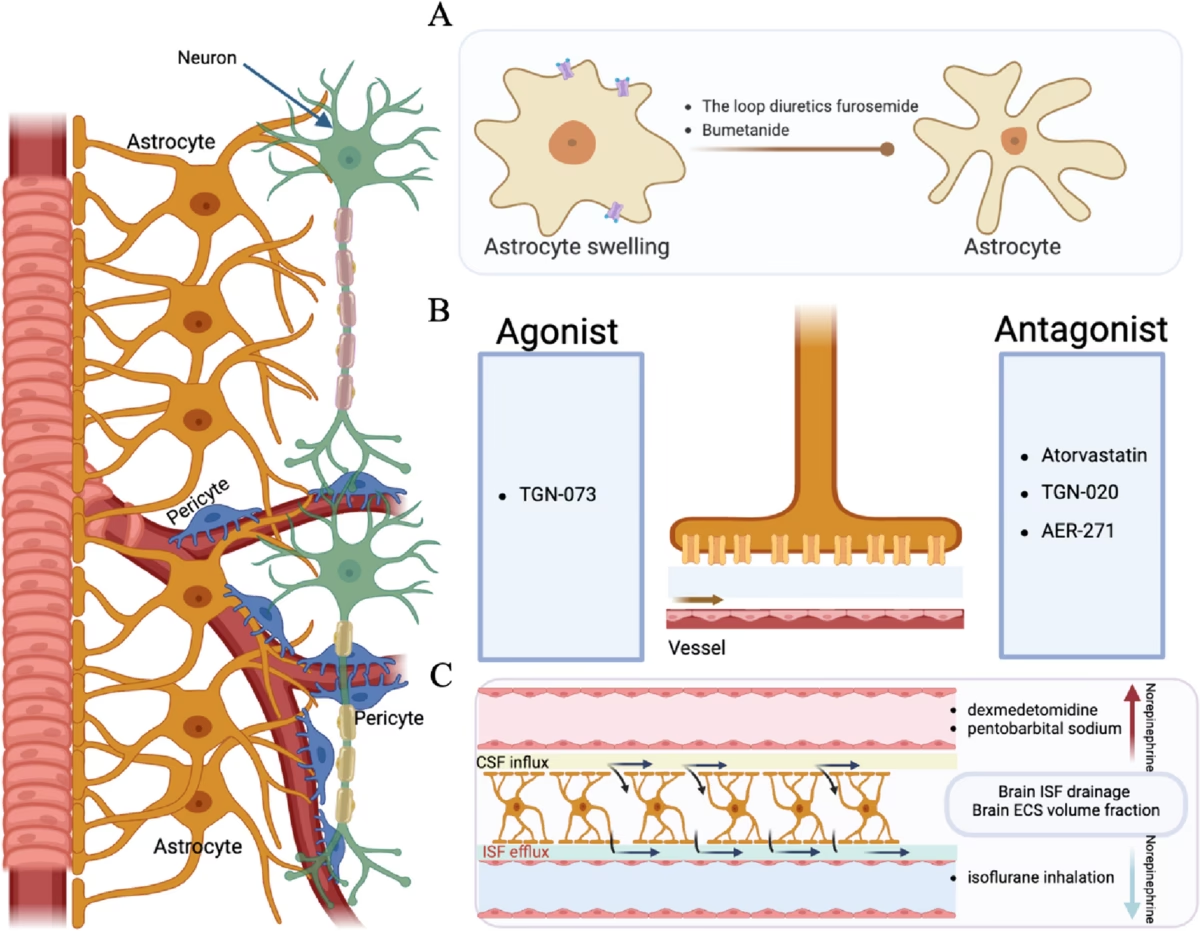
Recientemente, la hipótesis glifática ha revitalizado el interés en el flujo masivo. Propuesta por el grupo de Nedergaard, postula un sistema de transporte de fluidos y eliminación de desechos que involucra el flujo de agua a través de canales de acuaporina-4 en los pies terminales gliales perivasculares y la entrada de fluido desde los espacios perivasculares hacia el ECS, para luego salir por vías perivenosas profundas. Se sugirió que este sistema podría ser responsable de la eliminación de metabolitos tóxicos, y estudios han mostrado que el flujo (o la dispersión de trazadores) aumenta durante el sueño, correlacionándose con un aumento en la fracción de volumen del ECS en el estado de sueño/anestesiado en comparación con el estado de vigilia.
Sin embargo, la hipótesis glifática ha generado controversia. Una cuestión clave es discernir cuánto del movimiento observado de trazadores fluorescentes se debe realmente a un flujo masivo y cuánto a la difusión, que es dominante en distancias cortas. El número de Péclet (Pe) ayuda a estimar la relación entre transporte por flujo y por difusión. Para distancias típicas de observación en algunos experimentos glifáticos, Pe < 1, lo que sugiere que la difusión podría explicar gran parte de la dispersión observada.
Método Molécula Sonda Parámetros Medidos ¿En Tiempo Real? Notas de Resolución Espacial Ioniotoforesis en Tiempo Real (RTI) Iones pequeños (ej. TMA+) Fracción de Volumen (α), Tortuosidad (λ) Sí Macro (centenas de μm) promediando inhomogeneidades locales Imagenología Óptica Integrativa (IOI) Macromoléculas marcadas (ej. Dextranos, Proteínas) Coeficiente de Difusión Efectivo (D*), Tortuosidad (λ) Sí Macro (centenas de μm), permite estimar ancho del espacio Radiotrazadores Moléculas pequeñas (ej. Inulina, Sacarosa) Fracción de Volumen (α), Tortuosidad (λ) No (un punto por animal) Pobre (perfiles en tejido fijado) Seguimiento de Partículas Únicas Nanotubos de carbono, Puntos cuánticos Coeficiente de Difusión Local, Viscosidad, Variaciones de Ancho Sí Nano (seguimiento de partículas individuales) Imagenología de Anisotropía de Fluorescencia Moléculas pequeñas Viscosidad Local Sí Nano (inferido por rotación molecular) Preguntas Frecuentes sobre el Espacio Extracelular Cerebral
¿Qué tamaño tiene el espacio extracelular en el cerebro?
El espacio extracelular está formado por estrechos canales de aproximadamente 40 nanómetros de ancho. Aunque individualmente son diminutos, colectivamente ocupan alrededor del 20% del volumen total del tejido cerebral.

The ECS comprises the fluid-filled spaces external to cell membranes. This would encompass interstitial spaces between cells, the blood vessels, and perivascular spaces as well as the ventricular and subarachnoid spaces of the brain. ¿Cómo se comunican las células a través del espacio extracelular?
Las células se comunican mediante la difusión de moléculas señalizadoras (como iones, neurotransmisores o neuromoduladores) a través del líquido intersticial. Este tipo de comunicación se conoce como transmisión de volumen o extrasináptica.
¿Qué es la tortuosidad del espacio extracelular?
La tortuosidad (λ) es una medida de cuánto se ve obstaculizada la difusión de moléculas en el espacio extracelular en comparación con un medio libre. Un valor de λ=1.6 indica que las moléculas se mueven más lentamente debido a la compleja geometría del espacio y la presencia de la matriz extracelular.
¿Qué papel juega la matriz extracelular?
La matriz extracelular cerebral, compuesta por proteoglicanos y hialuronano, no solo proporciona soporte estructural, sino que también influye activamente en la difusión de moléculas, actuando como sitios de unión temporales o creando impedimentos físicos.
¿Qué es la hipótesis glifática?
La hipótesis glifática propone un sistema de eliminación de desechos en el cerebro que implica el flujo de líquido desde los espacios perivasculares hacia el espacio extracelular y su posterior drenaje. Es un área de investigación activa y debate sobre la contribución exacta del flujo masivo frente a la difusión en este proceso.
El estudio del espacio extracelular cerebral es un campo emocionante que continúa evolucionando. Las limitaciones de las técnicas de visualización directa han impulsado el desarrollo de métodos biofísicos sofisticados que nos permiten cuantificar sus propiedades y comprender su dinámica. A medida que emergen nuevas tecnologías, nuestra comprensión de este microambiente vital y sus complejas interacciones con las células y la matriz extracelular sin duda se profundizará, revelando aún más su importancia fundamental para la salud y la función del cerebro.
Si quieres conocer otros artículos parecidos a El Espacio Extracelular del Cerebro puedes visitar la categoría Neurociencia.
