En el vasto y complejo mundo de la biología y la medicina, los tejidos rara vez son homogéneos. Están compuestos por diversas poblaciones celulares, cada una con roles y características moleculares distintas. Estudiar la biología de un tipo celular específico dentro de un tejido complejo representa un desafío significativo. Aquí es donde técnicas avanzadas como la Microdisección por Captura Láser (LCM) entran en juego, ofreciendo una solución para aislar con una precisión sin precedentes las células de interés.
La LCM, también conocida como microdisección láser o microdisección asistida por láser, es una herramienta poderosa que permite a los investigadores y patólogos seleccionar y recolectar poblaciones celulares específicas, incluso células individuales, directamente de secciones de tejido o frotis celulares. Esta capacidad es crucial para obtener muestras puras para análisis moleculares posteriores, como genómica, transcriptómica o proteómica, donde la contaminación por células no deseadas puede enmascarar o distorsionar los resultados.
La necesidad de una técnica tan precisa surgió con el avance de la investigación. Si bien el uso de láseres en operaciones celulares se remonta a principios de la década de 1920, su aplicación como herramienta microquirúrgica se popularizó en los años 60. La evolución tecnológica ha sido clave, pasando de láseres UV iniciales a sistemas más refinados que combinan unidades láser con microscopios de alta resolución. Esta integración, junto con la mejora en las técnicas de preparación de tejidos, ha transformado la LCM en la herramienta indispensable que es hoy en día para aislar cantidades extremadamente pequeñas de tejido.
Principios y Funcionamiento de la LCM
Aunque existen diferentes sistemas de LCM, todos comparten principios fundamentales: la visualización, la selección y la captura del tejido de interés. El proceso comienza con la preparación de la muestra, que es un paso crítico. Los tejidos pueden ser fijados con formalina e incluidos en parafina (FFPE) o preparados como bloques congelados. Estas muestras se cortan en secciones delgadas (típicamente de 5 a 50 micrómetros de grosor) que se montan en portaobjetos especiales, a menudo recubiertos con una membrana, como la de polietileno naftalato (PEN). Se pueden aplicar diversas tinciones histológicas, como hematoxilina y eosina (H&E), hibridación in situ con fluorescencia (FISH) o inmunohistoquímica (IHC), para visualizar y diferenciar las poblaciones celulares.
Una vez preparada la muestra, se coloca bajo un microscopio conectado al sistema LCM. Utilizando una interfaz de software, el operador (a menudo un patólogo o citotecnólogo) visualiza la sección de tejido e identifica las células o regiones de interés. La selección se realiza dibujando digitalmente el contorno de estas áreas en la pantalla.

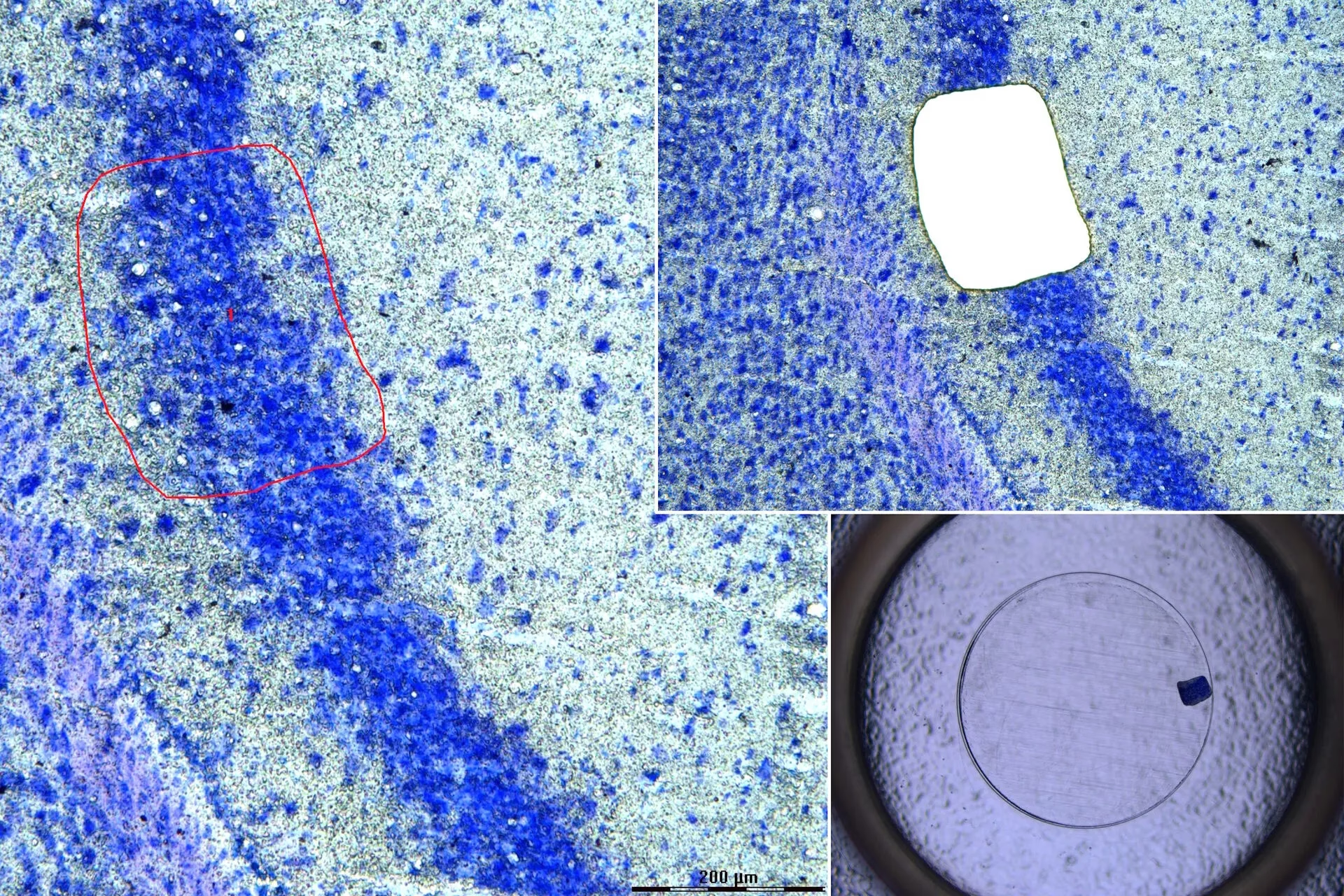
El siguiente paso es la excisión mediante láser. La mayoría de los sistemas modernos utilizan un láser pulsado de ultravioleta (UV) de 355 nm. El rayo láser, enfocado con gran precisión (ancho de corte generalmente inferior a 1 μm), sigue la trayectoria dibujada por el usuario, cortando la membrana del portaobjetos y el tejido seleccionado. La energía del láser UV es suficiente para cortar sin causar daños significativos a las moléculas celulares, lo cual es fundamental para los análisis posteriores. Esta capacidad de corte preciso asegura que solo las células seleccionadas sean separadas del tejido circundante no deseado.
Tras la excisión, el tejido diseccionado debe ser recolectado. Existen varias tecnologías de recolección:
- Catapulta por Presión Láser (LMPC): Utilizada por sistemas como Carl Zeiss PALM. Un pulso láser UV desenfocado genera una fuerza fotónica que impulsa el fragmento de tejido cortado hacia arriba, catapultándolo a un tubo colector colocado justo encima. Este método sin contacto evita problemas potenciales asociados con superficies adhesivas.
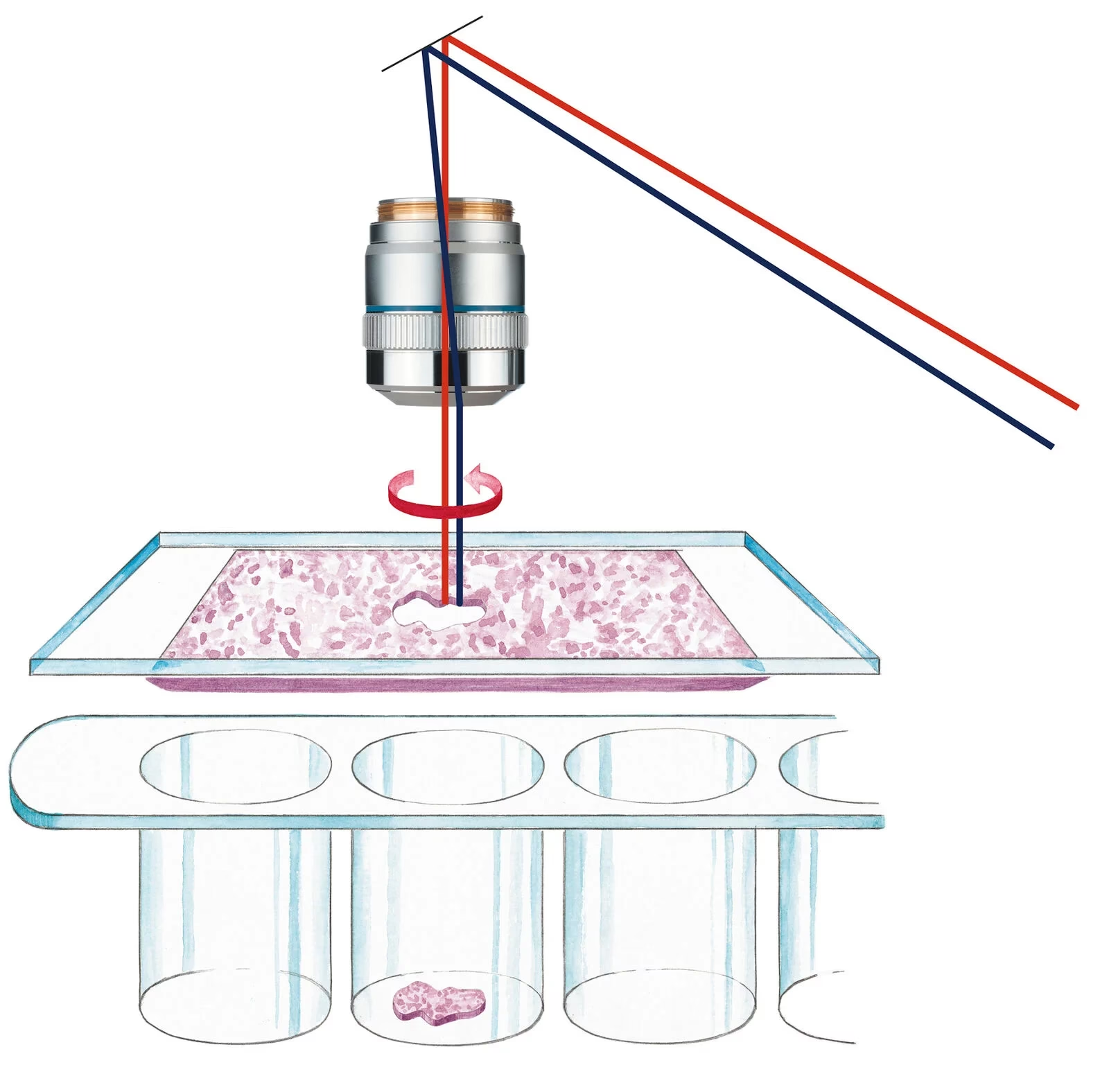
- Microdisección Asistida por Gravedad (GAM): En sistemas como Leica LMD, el portaobjetos se coloca invertido. El láser corta el tejido desde arriba, y el fragmento diseccionado cae por gravedad en un tubo colector o placa de pocillos situado debajo del portaobjetos. Esto permite el uso de consumibles de laboratorio estándar.
- Captura por Adhesión (Cut-and-Capture): Desarrollada por sistemas como Arcturus. Se coloca una tapa recubierta con un adhesivo especial sobre la sección de tejido. Un láser infrarrojo (IR) calienta suavemente el adhesivo, fusionándolo con el tejido subyacente. Un láser UV corta luego el tejido y la membrana. La entidad membrana-tejido queda adherida a la tapa y se retira. Aunque efectiva, el calor del láser IR (que puede alcanzar hasta 90°C) representa un riesgo potencial de degradación molecular, a diferencia del láser UV que mantiene una temperatura ambiente constante.
- Sistemas con Membrana Superior: Enfoques donde una membrana cubre la muestra, el láser corta la membrana y el tejido, y la muestra es recogida desde arriba con una tapa adhesiva.
- Portaobjetos con Recubrimiento de Transferencia de Energía: Portaobjetos especiales que, al ser impactados por el láser UV, convierten la energía en energía cinética, propulsando el tejido seleccionado hacia el colector. Son ventajosos para trabajos de proteómica ya que no autofluorescen.
La elección del sistema y el método de recolección puede depender del tipo de muestra y de los análisis posteriores previstos. Independientemente del método, el objetivo es obtener una población celular lo más pura posible para su posterior análisis, ya sea extracción de ADN, ARN o proteínas.
Ventajas de la Microdisección por Captura Láser
La LCM ha revolucionado la investigación biomédica al permitir el estudio de poblaciones celulares puras, superando la limitación de la heterogeneidad tisular. Entre sus numerosas ventajas se encuentran:
- Aislamiento de Alta Precisión: Permite separar con exactitud cantidades extremadamente pequeñas de células, desde poblaciones homogéneas dentro de un tejido heterogéneo hasta células individuales. La mejora en la resolución óptica incluso permite aislar orgánulos celulares en algunos casos.
- Preservación de la Morfología Tisular: A diferencia de otras técnicas de microdisección, la LCM puede realizar la disección manteniendo la morfología general del tejido circundante, lo cual es útil para la correlación histológica posterior.
- Rapidez (comparada con otros métodos de microdisección): Es un método de separación celular más rápido que algunas técnicas de microdisección manual, lo cual es crucial para preservar la integridad de las moléculas genómicas, especialmente el ARN, que es sensible a la degradación.
- Aislamiento de Células Vivas: Algunos sistemas permiten el aislamiento de células vivas directamente de placas de cultivo, posibilitando su posterior recultivo o clonación para estudios funcionales.
- Flexibilidad en Tipos de Muestra: Puede aplicarse a una amplia variedad de muestras, incluyendo tejidos FFPE, congelados, frotis celulares, preparaciones cromosómicas e incluso tejidos vegetales.
- Reducción de la Contaminación: Al aislar específicamente las células deseadas y utilizar métodos de recolección sin contacto (como la catapulta o la gravedad), se minimiza la contaminación cruzada con células no deseadas o componentes del estroma.
- Obtención de Material de Alta Calidad para Análisis 'Ómicos': La capacidad de obtener poblaciones celulares puras mejora significativamente la calidad y sensibilidad de los análisis posteriores de ADN, ARN y proteínas (genómica, transcriptómica, proteómica).
La posibilidad de trabajar con muestras FFPE archivadas, que son una fuente invaluable de material clínico, es otra ventaja clave, aunque requiere protocolos optimizados para mitigar el daño molecular causado por la fijación.
Desafíos y Desventajas de la LCM
A pesar de sus indudables beneficios, la LCM presenta ciertas limitaciones que pueden restringir su uso generalizado:
- Alto Costo Inicial: El sistema de LCM con el microscopio es una inversión muy significativa, que puede superar el millón de dólares.
- Costos de Consumibles: Los consumibles especializados, como los portaobjetos con membrana libre de nucleasas y los tubos de recolección, son considerablemente más caros que los materiales de laboratorio estándar.
- Proceso Lento y Dependiente del Usuario: La selección manual de las regiones de interés bajo el microscopio puede ser un proceso tedioso y que consume mucho tiempo, especialmente para muestras grandes o con poblaciones celulares dispersas. La velocidad y la precisión dependen en gran medida de la experiencia del operador (patólogo o citotecnólogo).
- Riesgo de Degradación Molecular: Aunque el láser UV es menos dañino que el IR, la exposición a fijadores y reactivos de tinción durante la preparación de la muestra, así como la deshidratación de las secciones (al no usar cubreobjetos ni medio de montaje), pueden afectar la calidad del ADN, ARN y proteínas. Se requieren protocolos optimizados para minimizar este riesgo.
- Necesidad de Formación y Resolución de Problemas: Lograr resultados de alta calidad con LCM requiere una cantidad sustancial de tiempo en formación y en la optimización de protocolos para cada tipo de tejido y análisis posterior.
- Cantidad de Material: Si bien es excelente para aislar células, la cantidad total de material (ADN, ARN, proteína) obtenida puede ser muy pequeña (nanogramos o microgramos), lo que requiere técnicas de análisis posteriores de alta sensibilidad. Para proteómica, a menudo se necesita una mayor cantidad de muestra que para genómica o transcriptómica.
Esfuerzos hacia la Automatización
Para abordar la desventaja del proceso lento y dependiente del usuario, se están realizando esfuerzos significativos para automatizar la selección de las regiones de interés. La LCM inmunoguiada utiliza la inmunotinción (con anticuerpos contra marcadores celulares específicos) para identificar automáticamente las células deseadas. Esto puede ser asistido por ordenador mediante algoritmos de reconocimiento de tinción o incluso basado en la expresión, donde un software semiautomático identifica y disecciona basándose en la intensidad de la tinción.
Otra técnica emergente es la cuantización vectorial espacialmente invariante, un algoritmo de reconocimiento de patrones que identifica tipos celulares basándose en características morfológicas (tamaño, forma, núcleo) sin necesidad de inmunotinción. También se están explorando enfoques como la microscopía infrarroja hiperespectral combinada con algoritmos de aprendizaje automático para identificar diferentes tipos de tejido basándose en sus espectros vibracionales, permitiendo una disección totalmente automatizada.
Estos avances en la automatización buscan hacer la LCM más rápida, reproducible y accesible para su uso en la práctica clínica diaria, más allá de su empleo predominante actual en la investigación.
Aplicaciones en Investigación Biomédica
La LCM es una herramienta versátil con aplicaciones en una amplia gama de áreas de investigación médica, incluyendo neurociencia, cáncer, ciencia forense, descubrimiento de biomarcadores y diagnóstico clínico. Sus aplicaciones se basan principalmente en el análisis molecular de los materiales aislados.
- Genómica y Transcriptómica: El ADN, ARN mensajero (mRNA) y microARN pueden extraerse de las células capturadas y utilizarse en técnicas como PCR cuantitativa en tiempo real, análisis de microarrays, secuenciación de ARN (RNA-seq) y secuenciación de próxima generación (NGS). Esto permite estudiar perfiles de expresión génica, mutaciones, variaciones en el número de copias y alteraciones epigenéticas en poblaciones celulares específicas.
- Proteómica: Las proteínas extraídas de los tejidos diseccionados por LCM pueden analizarse mediante electroforesis en gel 2D, espectrometría de masas (MS), Western blot y secuenciación de péptidos. Esto permite identificar y cuantificar el contenido proteico de poblaciones celulares específicas, lo cual es crucial para comprender las vías de señalización y la función celular. La combinación de LCM con espectrometría de masas (LCM-MS), incluyendo técnicas como MALDI-TOF MS, permite investigar el contenido celular en su contexto morfológico, incluso a resolución de célula única.
Aplicaciones en Neurociencia
En neurociencia, la LCM es particularmente valiosa debido al fenómeno de la 'vulnerabilidad selectiva' en muchas enfermedades neurodegenerativas. Esta característica implica que solo ciertos tipos de neuronas o células gliales se degeneran o disfuncionan, mientras que las células circundantes permanecen relativamente ilesas. Estudiar los mecanismos precisos de degeneración requiere el análisis de las células afectadas, lo cual es difícil en tejidos heterogéneos. La LCM resuelve este problema al permitir aislar específicamente las células vulnerables de muestras post-mortem o modelos animales.

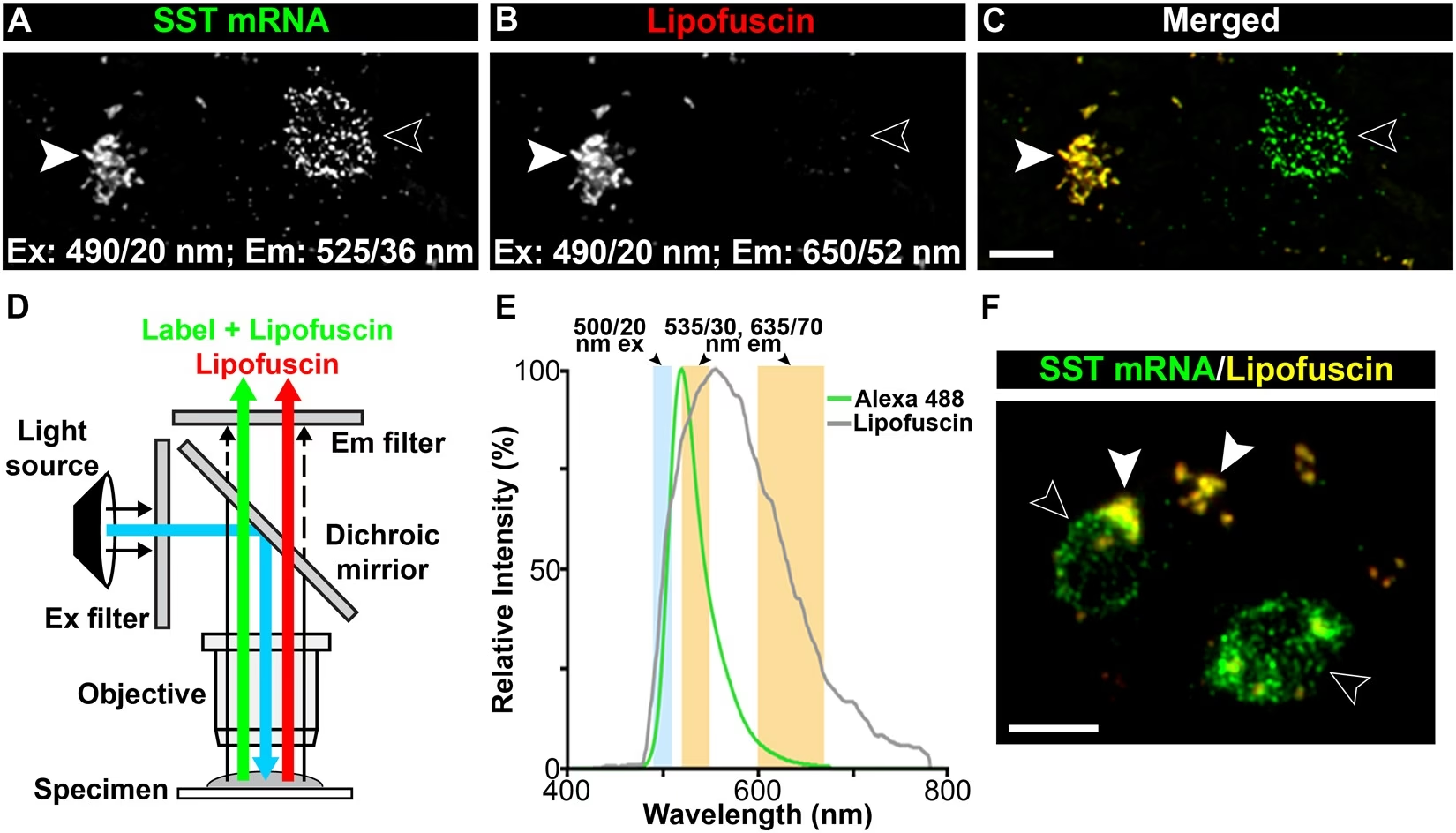
- Enfermedad de Alzheimer: La acumulación de placas amiloides es un sello distintivo de esta enfermedad. La LCM se ha utilizado para aislar estas placas (etiquetadas con tinciones específicas) de muestras post-mortem y analizar su composición proteica mediante LCM-MS. Esto ha permitido identificar nuevas proteínas enriquecidas en las placas y comparar perfiles proteicos entre muestras humanas y modelos murinos, arrojando luz sobre los posibles mecanismos de degeneración neurítica.
- Diagnóstico en Terapia con Células Madre: La LCM ha demostrado ser útil en el diagnóstico, por ejemplo, para determinar el origen de tumores desarrollados tras terapias con células madre. Al aislar núcleos celulares de las células tumorales mediante LCM, se puede realizar análisis genómico (como genotipado de SNP) para comparar el ADN del tumor con el del paciente y el donante, confirmando si el tumor se originó de las células trasplantadas.
- Degeneración Retiniana: En modelos de enfermedades retinianas, como la maculopatía telangiectásica tipo 2 (MacTel Tipo 2), donde la pérdida de células de Müller contribuye a la degeneración de fotorreceptores, la LCM se ha utilizado para aislar áreas específicas de ablación de células de Müller. El análisis genómico posterior de estas áreas ha revelado alteraciones en vías metabólicas clave, proporcionando información sobre los mecanismos moleculares de la degeneración causada por la disfunción glial primaria.
Aplicaciones en Cáncer
En la investigación del cáncer, especialmente en tumores sólidos como el cáncer de pulmón, la heterogeneidad celular (mezcla de células tumorales, estroma, células inmunes, etc.) es un obstáculo importante para el análisis molecular preciso. La LCM permite aislar poblaciones de células tumorales puras de biopsias pequeñas o muestras citológicas, mejorando la sensibilidad de las pruebas de mutación (EGFR, KRAS, etc.) y análisis de expresión génica o proteica, que son cruciales para la medicina de precisión.
Tabla Comparativa: Ventajas y Desventajas de la LCM
| Ventajas | Desventajas |
|---|---|
| Aislamiento a nivel de célula única | Alto costo de adquisición y consumibles |
| Combinación con técnicas de alta resolución (ej. MS) | Proceso que consume tiempo (selección) |
| Selección de ROI semi/totalmente automatizada (sistemas avanzados) | Posible degradación por calor (láser IR) o procesamiento |
| Flujo de trabajo digitalizado e integrado (potencial futuro) | Selección tediosa y dependiente del usuario (métodos manuales) |
| Permite el estudio de poblaciones celulares puras | Requiere experiencia del operador |
| Aplicable a diversos tipos de muestras (FFPE, congelado, vivo) | Presencia de nucleasas/proteasas tisulares puede afectar la calidad |
| Preserva la morfología tisular circundante | Problemas técnicos y de calidad por pasos de tinción (LCM inmunoguiada) |
| Más rápido que algunos métodos manuales de microdisección | Cantidad limitada de material para análisis posteriores (requiere métodos sensibles) |
Preguntas Frecuentes (FAQ) sobre LCM
- ¿Qué tipos de muestras se pueden usar con LCM?
La LCM es compatible con una amplia variedad de muestras, incluyendo secciones de tejido fijadas con formalina e incluidas en parafina (FFPE), secciones congeladas, frotis celulares, preparaciones cromosómicas e incluso células o tejidos vivos en cultivo. - ¿La LCM daña las células o sus moléculas (ADN, ARN, proteínas)?
Los sistemas modernos, especialmente aquellos que utilizan láseres UV pulsados, están diseñados para minimizar el daño. El corte láser UV es muy preciso y el pulso es extremadamente corto. Sin embargo, la calidad del material molecular también depende de la preparación inicial de la muestra (fijación, tinción) y del método de recolección (el calor del láser IR puede ser más problemático). - ¿Cuál es la diferencia principal entre los sistemas de láser UV e IR?
Los sistemas de láser UV se utilizan principalmente para cortar y a veces para catapultar el tejido, manteniendo la muestra a temperatura ambiente. Los sistemas de láser IR se utilizan a menudo para fundir un adhesivo y capturar el tejido. La principal diferencia es la generación de calor; el láser IR puede aumentar la temperatura significativamente (hasta 90°C), lo que aumenta el riesgo de degradación molecular, mientras que el láser UV minimiza este riesgo. - ¿La LCM es una técnica cara?
Sí, la LCM es una técnica costosa. La inversión inicial en el equipo es muy alta, y los consumibles especializados también tienen un precio considerablemente mayor que los materiales de laboratorio estándar. - ¿Es la LCM un proceso rápido?
Comparada con algunas técnicas de microdisección manual, la LCM puede ser más rápida en el corte. Sin embargo, la fase de selección de las células o regiones de interés bajo el microscopio, que a menudo se realiza manualmente, puede ser muy laboriosa y consumir mucho tiempo, especialmente en muestras complejas. Las técnicas de automatización buscan acelerar este paso.
Conclusión
La Microdisección por Captura Láser es una técnica excepcionalmente potente y útil en diversas áreas de la investigación biomédica, especialmente donde el aislamiento preciso de poblaciones celulares puras de muestras heterogéneas es fundamental. Su capacidad para trabajar con muestras pequeñas y preservar la integridad molecular la hace indispensable para análisis 'ómicos' de alta sensibilidad.
Si bien el alto costo, el tiempo de procesamiento (particularmente la selección manual) y los desafíos en la preparación de muestras siguen siendo limitaciones, los avances continuos en la automatización y la integración con otras técnicas analíticas, como la espectrometría de masas o la secuenciación de próxima generación, están ampliando su accesibilidad y potencial. En campos como la neurociencia, donde la vulnerabilidad selectiva es común, la LCM es quizás la herramienta más ventajosa para desentrañar los mecanismos moleculares subyacentes a las enfermedades.
Si quieres conocer otros artículos parecidos a Microdisección Láser: Precisión Celular puedes visitar la categoría Neurociencia.