La tetrodotoxina (TTX) es una de las neurotoxinas más potentes conocidas, infame por su presencia en el pez globo (fugu), un manjar en algunas culturas que, si se prepara incorrectamente, puede ser mortal. Sin embargo, más allá de su notoriedad tóxica, la TTX es una herramienta invaluable en la investigación neurocientífica. Su mecanismo de acción altamente específico sobre los canales de sodio dependientes de voltaje la convierte en una sonda química esencial para estudiar la excitabilidad neuronal y desentrañar los secretos de la transmisión nerviosa.
- ¿Qué es la Tetrodotoxina (TTX)?
- El Mecanismo de Acción: Un Bloqueo Específico de Canales de Sodio
- Canales de Sodio: Sensibles vs. Resistentes a TTX
- TTX como Herramienta Fundamental en Neurociencia
- TTX y la Epilepsia: Un Modelo Experimental
- Toxicidad en Humanos: Un Riesgo Letal
- Manejo y Tratamiento de la Intoxicación por TTX
- Prevención: La Mejor Estrategia
¿Qué es la Tetrodotoxina (TTX)?
La tetrodotoxina es una molécula compleja que se encuentra en una sorprendente diversidad de organismos, tanto marinos como terrestres. Si bien el pez globo es su fuente más conocida, también se ha aislado de tritones (como el género Taricha), pulpos de anillos azules, cangrejos, estrellas de mar, caracoles marinos y gusanos, entre otros. Contrario a la creencia popular, la mayoría de estos animales no producen la toxina por sí mismos. La TTX es biosintetizada principalmente por ciertas especies de bacterias, como Vibrio, Aeromonas, Pseudomonas y Pseudoalteromonas. Estos microorganismos viven a menudo en simbiosis con los animales o se acumulan en ellos a través de la cadena alimentaria. Esta ruta bacteriana explica su amplia distribución en especies filogenéticamente distantes.
La toxina actúa como un mecanismo de defensa contra depredadores para muchos animales que la portan. Sin embargo, algunos depredadores, como ciertas serpientes de cascabel que se alimentan de tritones tóxicos, han desarrollado resistencia a la TTX a través de mutaciones en sus propios canales de sodio o mediante proteínas de unión a la toxina.
El Mecanismo de Acción: Un Bloqueo Específico de Canales de Sodio
En el corazón de la función neuronal se encuentra la generación de potenciales de acción, impulsos eléctricos que permiten a las neuronas comunicarse. Este proceso depende en gran medida del flujo de iones de sodio a través de canales específicos en la membrana celular: los canales de sodio dependientes de voltaje. Estos canales se abren en respuesta a cambios en el potencial de membrana, permitiendo una rápida entrada de Na+ que despolariza la célula y propaga la señal eléctrica.
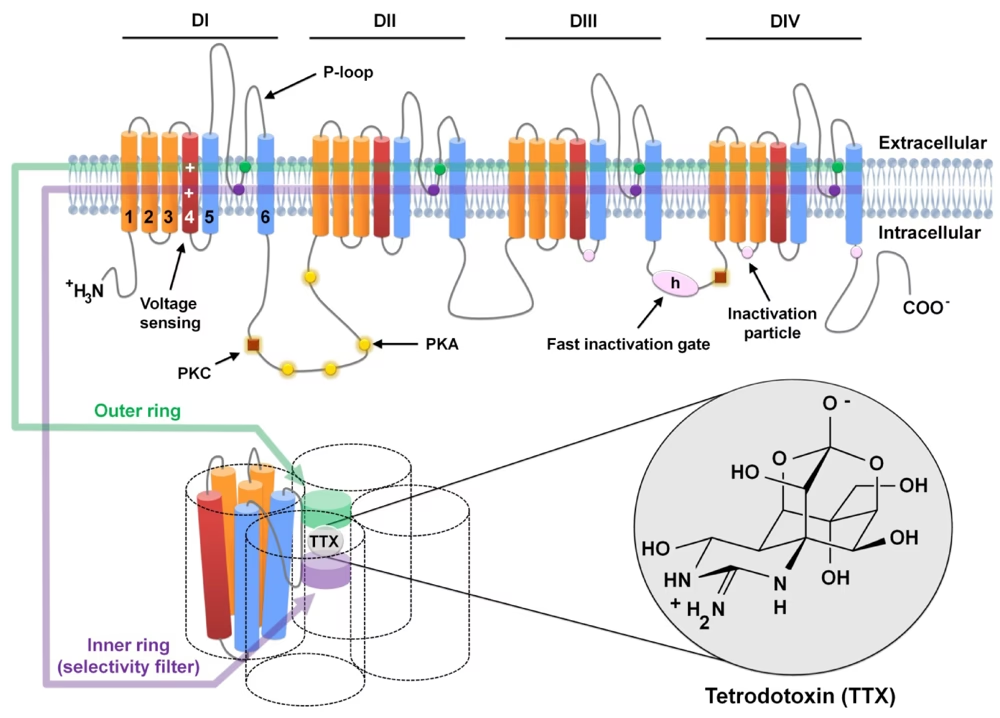
La TTX ejerce su efecto tóxico y su utilidad científica al bloquear de manera sumamente potente y selectiva estos canales de sodio. Lo hace uniéndose a un sitio específico en la abertura extracelular del poro del canal, conocido como el filtro de selectividad (sitio 1). La molécula de TTX, con su grupo guanidinio cargado positivamente, encaja en la boca del poro e interactúa con residuos de aminoácidos cargados negativamente, actuando como un tapón que impide físicamente el paso de los iones de sodio a través del canal. Es crucial entender que la TTX bloquea el canal solo desde el exterior de la membrana nerviosa. A diferencia de muchos anestésicos locales que pueden actuar desde el interior, la TTX es demasiado grande para penetrar el canal una vez que está dentro de la célula. Además, y esto es clave para su uso como herramienta, la TTX no afecta el mecanismo de compuerta del canal; simplemente bloquea el flujo de iones una vez que la compuerta se abre. Esto permite a los investigadores estudiar otras propiedades del canal sin la interferencia del flujo de sodio.
Canales de Sodio: Sensibles vs. Resistentes a TTX
Uno de los descubrimientos importantes posibilitados por la TTX es la existencia de diferentes subtipos de canales de sodio dependientes de voltaje en mamíferos. No todos son igualmente sensibles a la toxina:
- Canales Sensibles a TTX (TTX-S): La mayoría de los canales de sodio en el sistema nervioso central y periférico son altamente sensibles a la TTX, siendo bloqueados a concentraciones muy bajas (del orden de 1-10 nM). Estos incluyen los subtipos NaV1.1, NaV1.2, NaV1.3, NaV1.6 y NaV1.7. También el canal NaV1.4 del músculo esquelético es TTX-S.
- Canales Resistentes a TTX (TTX-R): Algunos canales requieren concentraciones mucho más altas de TTX (del orden de µM) para ser bloqueados. Estos incluyen el canal NaV1.5, que es el principal canal de sodio en el músculo cardíaco, y los canales NaV1.8 y NaV1.9, encontrados predominantemente en neuronas sensoriales del ganglio de la raíz dorsal (DRG).
La existencia de canales TTX-R en las neuronas sensoriales del DRG ha despertado un gran interés, ya que estos canales están implicados en la transmisión de sensaciones de dolor. La búsqueda de compuestos que puedan bloquear selectivamente los canales NaV1.8 o NaV1.9 sin afectar los canales TTX-S generalizados en el sistema nervioso es un área activa de investigación para el desarrollo de nuevos analgésicos.

TTX como Herramienta Fundamental en Neurociencia
Desde su descubrimiento como bloqueador de canales en la década de 1960, la TTX se convirtió rápidamente en una herramienta indispensable en fisiología y farmacología. Permite a los investigadores aislar y estudiar las corrientes de iones de potasio u otras corrientes iónicas sin la interferencia de la gran corriente de sodio. Su alta afinidad y especificidad han sido cruciales para:
- Cuantificar la densidad de canales de sodio en diferentes tejidos nerviosos y musculares (aunque las mediciones iniciales con bioensayos subestimaron la densidad real, estudios posteriores con saxitoxina tritiada, otra toxina que se une al mismo sitio, proporcionaron valores más precisos).
- Identificar y caracterizar los diferentes subtipos de canales de sodio (TTX-S vs TTX-R) y sus propiedades biofísicas.
- Estudiar la estructura molecular del poro del canal de sodio, ya que el sitio de unión de la TTX se encuentra en el filtro de selectividad formado por los bucles P de las cuatro subunidades.
- Silenciar selectivamente la actividad eléctrica dependiente de sodio en cultivos celulares o preparaciones de tejido, permitiendo el estudio de otras formas de señalización celular.
TTX y la Epilepsia: Un Modelo Experimental
Curiosamente, la infusión de TTX en regiones cerebrales como la corteza o el hipocampo en ratas jóvenes (PN16-20) ha demostrado inducir un fenotipo epiléptico. Alrededor del 31.4% de las ratas infusionadas manifiestan espasmos conductuales breves. Estos espasmos se describen como muy cortos (1-2 segundos), extensor o flexor del cuerpo, a veces con movimientos de las patas delanteras. Pueden ser simétricos o asimétricos, y su severidad varía desde un simple tirón hasta una contracción intensa que causa la caída del animal. Su frecuencia aumenta con el tiempo y pueden persistir meses después de retirar la infusión de TTX. El correlato electroencefalográfico (EEG) ictal incluye una onda lenta generalizada de alta amplitud seguida de una atenuación generalizada del voltaje (electrodecremento) con actividad rápida superpuesta, durando entre 1-10 segundos. La correlación electroclínica no siempre está presente, y la mayoría de los espasmos ocurren durante el estado de vigilia o excitación.
Además de los espasmos, también se observan crisis focales, que pueden aparecer tan pronto como 2 días después del inicio del registro de EEG. Conductualmente, se describen como postura tónica de la cabeza y parte superior del tronco, clonus predominantemente en la pata delantera izquierda y masticación excesiva. Inicialmente duran un promedio de 3 segundos, pero pueden prolongarse (hasta ~89 segundos) meses después de cesar la infusión, terminando en clonus bilateral, levantamiento y caída.
El EEG interictal (entre crisis) muestra puntas y ondas agudas multifocales, más prevalentes durante el sueño NREM y contralaterales al sitio de infusión. En ratas con espasmos inducidos por TTX, se observa un fondo de EEG caótico de alta amplitud durante el sueño NREM, a veces asimétrico. Este modelo se considera relevante para estudiar la hipsarritmia, un patrón de EEG caótico asociado con ciertos síndromes epilépticos infantiles severos como el Síndrome de West.
Toxicidad en Humanos: Un Riesgo Letal
La TTX es extremadamente tóxica para los mamíferos. La dosis letal media (LD50) oral en ratones es del orden de 334 µg/kg, y por vía intravenosa es aún menor (8 µg/kg en ratones). Puede ingresar al cuerpo por ingestión, inyección (como la mordedura de pulpos de anillos azules) o a través de la piel erosionada. El envenenamiento más común ocurre por el consumo de pez globo, especialmente si sus órganos (hígado, ovarios) no se retiran adecuadamente, ya que concentran la toxina. La TTX es resistente al calor, por lo que cocinar no la destruye.
Los síntomas suelen aparecer rápidamente, a menudo en 30 minutos, aunque pueden tardar varias horas. La gravedad varía según la dosis. La escala de Fukuda y Tani clasifica la toxicidad en 4 grados:
- Grado 1: Parestesias y adormecimiento alrededor de la boca (síntoma inicial clásico), con o sin síntomas gastrointestinales (náuseas, vómitos, diarrea, dolor abdominal).
- Grado 2: Adormecimiento facial, dificultad para hablar (lenguaje arrastrado), parálisis motora leve y descoordinación, pero con reflejos normales.
- Grado 3: Parálisis flácida generalizada, pérdida del habla (afonía), insuficiencia respiratoria, pupilas fijas o dilatadas (en paciente consciente).
- Grado 4: Insuficiencia respiratoria severa con hipoxia, bradicardia (ritmo cardíaco lento), hipotensión, arritmias cardíacas e inconsciencia (coma).
La muerte, si ocurre, suele ser secundaria a la insuficiencia respiratoria debido a la parálisis del diafragma y los músculos intercostales, o al colapso cardiovascular. Lo trágico es que la víctima puede permanecer consciente y lúcida hasta poco antes de morir, a pesar de la parálisis total.

Manejo y Tratamiento de la Intoxicación por TTX
Actualmente, no existe un antídoto específico aprobado para la intoxicación por TTX. El manejo es fundamentalmente de soporte. La prioridad es asegurar la vía aérea y la ventilación, a menudo requiriendo intubación y ventilación mecánica hasta que la toxina sea eliminada del cuerpo. Si la ingestión fue reciente (dentro de los 60 minutos) y el paciente está consciente, se pueden considerar medidas de descontaminación gástrica como el lavado gástrico o la administración de carbón activado para intentar reducir la absorción.
Los pacientes deben ser monitoreados de cerca en una unidad de cuidados intensivos debido al riesgo de progresión rápida o aparición tardía de síntomas severos, incluyendo complicaciones cardíacas como bradicardia e hipotensión. Se administran fluidos intravenosos y, si es necesario, agentes alfa-adrenérgicos para mantener la presión arterial. Se ha investigado el uso de agentes anticolinesterasa como la neostigmina, pero la evidencia actual es insuficiente para recomendar su uso rutinario. La utilidad de la hemodiálisis para eliminar la TTX es conflictiva en la literatura, aunque algunos informes sugieren un posible beneficio en pacientes con disfunción renal.
A pesar de la gravedad potencial, con un soporte vital adecuado y oportuno, la mayoría de los pacientes que superan las primeras 24 horas suelen recuperarse completamente sin secuelas neurológicas permanentes.
Prevención: La Mejor Estrategia
Dado que no hay antídoto y el tratamiento es solo de soporte, la prevención es crucial. La forma más efectiva de evitar la intoxicación por TTX es abstenerse de consumir animales que se sabe que la contienen, especialmente pez globo, a menos que sea preparado por chefs altamente capacitados y con licencia en establecimientos regulados. También es importante evitar la manipulación o el consumo de otros animales conocidos por ser tóxicos, como ciertos tritones, cangrejos o moluscos, que no forman parte de la dieta habitual pero pueden ser fuentes de exposición accidental.
Canales de Sodio Sensibles vs. Resistentes a TTX
| Característica | Canales Sensibles a TTX (TTX-S) | Canales Resistentes a TTX (TTX-R) |
|---|---|---|
| Concentración de Bloqueo por TTX | Baja (nM) | Alta (µM) |
| Subtipos Comunes | NaV1.1, 1.2, 1.3, 1.4, 1.6, 1.7 | NaV1.5, 1.8, 1.9 |
| Localización Principal | Sistema Nervioso Central y Periférico, Músculo Esquelético | Músculo Cardíaco, Neuronas Sensoriales (DRG), Sistema Nervioso Periférico |
| Velocidad de Cinética | Generalmente más rápidas | Generalmente más lentas (activación/inactivación) |
| Relevancia Clínica/Investigación | Conducción nerviosa general, excitabilidad. Herramienta para estudio neuronal. | Dolor (NaV1.8, 1.9), función cardíaca (NaV1.5). Desarrollo de analgésicos selectivos. |
Preguntas Frecuentes sobre la TTX
¿Dónde se encuentra principalmente la TTX?
Aunque es famosa por el pez globo (fugu), la TTX se encuentra en muchos otros animales, como tritones, pulpos de anillos azules, cangrejos y estrellas de mar. La toxina es producida principalmente por bacterias y se acumula en estos animales a través de la cadena alimentaria.

¿Cómo mata la TTX a una persona?
La TTX bloquea los canales de sodio en las células nerviosas y musculares, impidiendo la transmisión de señales. Esto causa parálisis, incluyendo la de los músculos respiratorios (diafragma y músculos intercostales), llevando a la asfixia. También puede afectar el corazón y causar colapso cardiovascular.
¿Existe un antídoto para la intoxicación por TTX?
No, actualmente no existe un antídoto específico aprobado para uso humano. El tratamiento se basa en medidas de soporte vital, como mantener la respiración y la circulación, hasta que el cuerpo elimine la toxina.
¿Por qué algunos animales que contienen TTX no se envenenan?
Estos animales han desarrollado resistencia a la TTX a través de mutaciones genéticas en sus propios canales de sodio, que alteran el sitio de unión de la toxina, o mediante la producción de proteínas que se unen a la TTX y la secuestran.
¿Puede la TTX causar convulsiones o epilepsia?
Sí, en modelos experimentales con ratas, la infusión de TTX en ciertas áreas del cerebro puede inducir espasmos y crisis epilépticas focales, y el patrón de EEG asociado se asemeja a la hipsarritmia observada en algunos síndromes epilépticos humanos.
Si quieres conocer otros artículos parecidos a TTX: La Neurotoxina que Silencia Neuronas puedes visitar la categoría Neurociencia.
