La esquizofrenia es una condición de salud mental compleja y grave que impacta profundamente la manera en que una persona piensa, siente y se comporta. Se manifiesta a menudo como una mezcla de alucinaciones, delirios, pensamiento y comportamiento desorganizados. Quienes la padecen pueden perder el contacto con la realidad, lo que dificulta enormemente la vida diaria. Aunque las causas exactas aún se investigan, la neurociencia ha arrojado luz significativa sobre los factores neurológicos que contribuyen a su desarrollo y manifestación.

- Un Trastorno Multifactorial con Base Neurológica
- El Papel de la Genética
- Química Cerebral y Neurotransmisores Clave
- Alteraciones Estructurales en el Cerebro
- Redes Cerebrales y Fisiopatología
- Neurobiología del Inicio y la Progresión
- Deterioro Cognitivo y Función Cerebral
- Enfoques Farmacológicos
- Preguntas Frecuentes sobre las Causas Neurológicas
- Comparativa: Síntomas Positivos vs. Negativos
Un Trastorno Multifactorial con Base Neurológica
No se conoce una única causa para la esquizofrenia. Sin embargo, los investigadores coinciden en que una combinación de factores genéticos, la química cerebral y el entorno juegan un papel crucial. Los estudios de neuroimagen han revelado consistentemente cambios en la estructura cerebral y el sistema nervioso central de las personas con esquizofrenia, lo que subraya que es, fundamentalmente, una enfermedad cerebral.
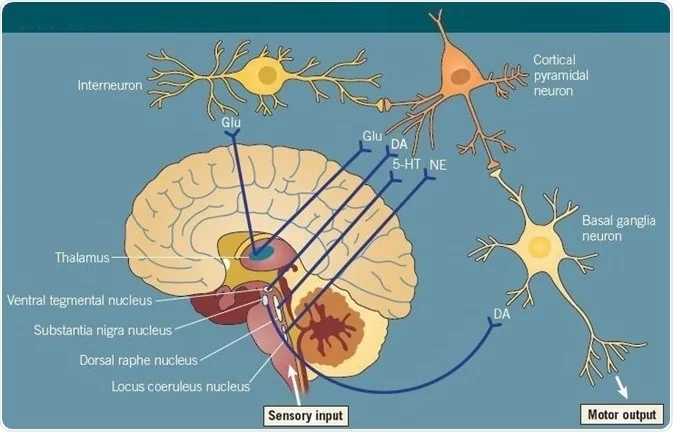
La comprensión de la fisiopatología de la esquizofrenia es compleja y ha sido objeto de estudio durante años. Aunque muchos factores aún están por descubrirse, la investigación actual apunta a desregulaciones específicas a nivel molecular, celular y de redes neuronales.
El Papel de la Genética
La esquizofrenia tiene un modo de herencia complejo que involucra múltiples genes, procesos biológicos y factores ambientales. Existe una contribución significativa de factores genéticos a su etiología. Si bien el vínculo exacto entre los múltiples genes y las alteraciones específicas de ADN y proteínas no se ha identificado completamente, estudios genómicos a gran escala han mostrado variantes específicas de ADN y cómo diversas alelos de riesgo contribuyen a la enfermedad.
Se considera un síndrome altamente poligénico, con cientos o incluso miles de loci genéticos distintos implicados. Estudios de asociación de genoma completo (GWAS) han identificado más de 100 loci genéticos distintos con alelos comunes de diversos efectos. Curiosamente, el riesgo genético de la enfermedad parece ser altamente pleiotrópico, compartiendo variantes de riesgo comunes con el trastorno bipolar, el trastorno depresivo mayor y el trastorno del espectro autista.
Otro hallazgo significativo de los estudios GWAS es la existencia de múltiples variantes correlacionadas en el complejo mayor de histocompatibilidad (MHC). Estas variantes de MHC están asociadas con la inmunidad adquirida, sugiriendo que los procesos inmunes e inflamatorios están involucrados en las etapas de desarrollo de la esquizofrenia, como durante el embarazo, la adolescencia y la edad adulta. Las moléculas de MHC de clase I regulan componentes del desarrollo cerebral como la formación de sinapsis, el crecimiento de neuritas y la plasticidad homeostática.
Un enfoque alternativo para identificar los genes implicados es el concepto de 'endofenotipo', que son biomarcadores cuantitativos de enfermedades heredables que conectan los síntomas conductuales con fenotipos específicos y genes de riesgo. La disfunción del sistema nervioso central, incluyendo cambios en el lóbulo frontal (memoria, funciones ejecutivas) y el lóbulo temporal (lenguaje, percepción auditiva, memoria episódica), está predispuesta por muchos loci genéticos sospechosos. Se han identificado asociaciones prometedoras con genes candidatos como COMT, DISC1, RGS4, PPP3CC, ZDHHC8, AKT1, neuregulina, disbindina, G72/G30, TRAR4 y genes del receptor nicotínico alfa-7.
Estos genes están asociados con la regulación de la dopamina, contribuyendo a la causa subyacente de la esquizofrenia. La evidencia de vinculación es más fuerte para dos genes: la proteína de unión a distrofina 1 (DTNBP1) y la neuregulina 1 (NRG1). Ambos se expresan en las sinapsis del sistema nervioso central y tienen un impacto en la neurotransmisión de glutamato, también implicada en la esquizofrenia.
Química Cerebral y Neurotransmisores Clave
Los síntomas positivos, negativos y cognitivos de la esquizofrenia se han asociado con muchos neurotransmisores, pero la disfunción de la dopamina subcortical sigue siendo el factor clave en los síntomas psicóticos. La disfunción presináptica de la dopamina parece mediar la psicosis en la esquizofrenia. Estimulantes como las anfetaminas potencian el efecto de la dopamina y pueden inducir síntomas psicóticos en individuos sanos. Las personas con esquizofrenia son más sensibles a estos efectos debido a un mayor contenido de dopamina sináptica subcortical, síntesis de dopamina y liberación anormalmente alta tras la administración de anfetaminas.
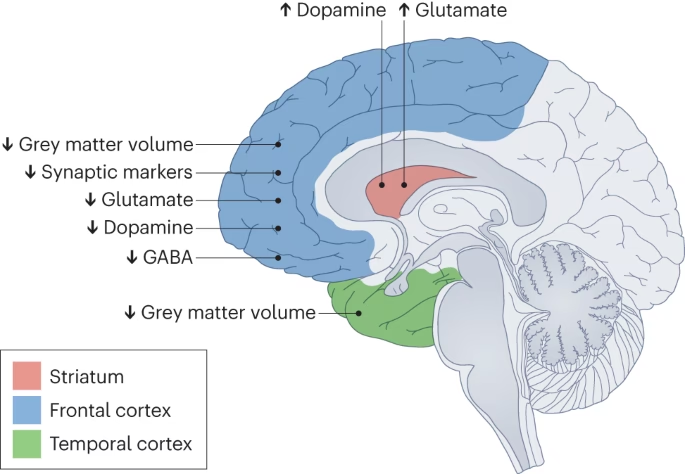
Estudios de tomografía por emisión de positrones (PET) han localizado este aumento del contenido de dopamina sináptica en el estriado. Las alteraciones en la función de la dopamina dentro del estriado en pacientes con esquizofrenia se asocian con delirios y psicosis.
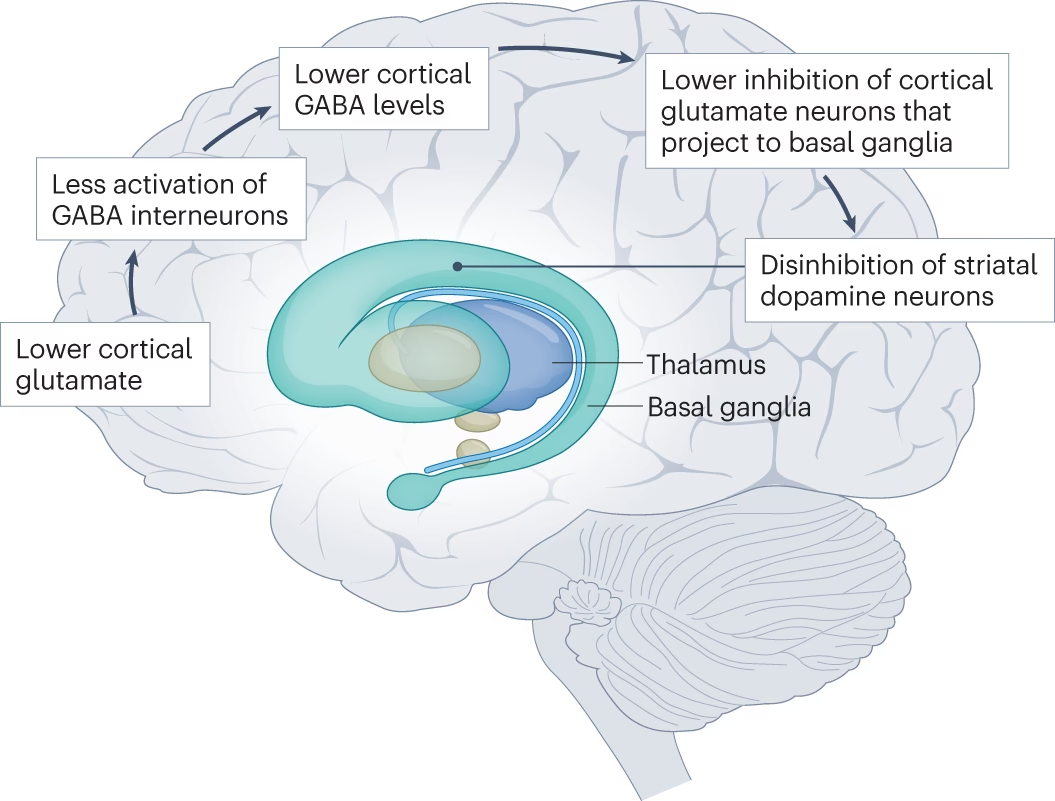
Además de la dopamina, otros neurotransmisores están implicados. Las neuronas dopaminérgicas también liberan cotransmisores como el glutamato y el ácido gamma-aminobutírico (GABA). El glutamato, en la vía excitatoria, y el GABA, en la vía inhibitoria, transmiten patrones de actividad neuronal dopaminérgica al estriado. Los antagonistas del receptor N-metil-D-aspartato (NMDA), como la ketamina y la fenciclidina (PCP), pueden alterar el circuito del tálamo y provocar disfunción cognitiva y síntomas psicóticos. Las personas con esquizofrenia son más sensibles a estos efectos, lo que sugiere que la hipofunción de los receptores NMDA podría estar asociada con la patogénesis. El tratamiento con moduladores de receptores NMDA, como D-serina, glicina y sarcosina, podría ser beneficioso, especialmente para los síntomas negativos.
Las interneuronas GABAérgicas, como las neuronas candelabro, muestran una reducción en la inmunotinción del transportador de GABA, lo que podría estar relacionado con una disminución en la señalización del factor neurotrófico derivado del cerebro (BDNF) o la hipofunción del receptor NMDA. El BDNF potencia la transmisión glutamatérgica y reduce la transmisión GABAérgica, causando alteraciones en la supervivencia neuronal y la función del SNC. Aún no está claro hasta qué punto estos cambios contribuyen a la fisiopatología.
Alteraciones Estructurales en el Cerebro
La esquizofrenia es conocida por presentar cambios neuroanatómicos a lo largo del tiempo. Diversas regiones cerebrales están implicadas, afectando consistentemente la materia gris. El uso extendido de resonancia magnética (MRI) ha mostrado evidencia de volúmenes reducidos de materia gris en los lóbulos prefrontal, medial y temporal superior. Esto podría explicar el deterioro de la memoria episódica y las fluctuaciones en la toma de decisiones a medida que progresa la enfermedad.
Además de los cambios en la materia gris, la materia blanca también se ve afectada a medida que la esquizofrenia se vuelve crónica. La resonancia magnética con tensor de difusión (DTI) se utiliza para visualizar la integridad estructural de la materia blanca mediante patrones de difusión del agua. La anisotropía fraccional (FA) evalúa la integridad de la mielinización. Estudios en esquizofrenia muestran una disminución de la FA en tractos principales como el fascículo longitudinal superior, el cíngulo, el fascículo uncinado, el fascículo longitudinal inferior y el hipocampo. Como estas vías colaboran en redes neuronales, el aumento de la desmielinización observado puede impactar muchas habilidades cognitivas.
Estudios con tomografía computarizada (TC) han demostrado una pérdida generalizada de tejido cerebral junto con un aumento ventricular en pacientes esquizofrénicos. Los ventrículos laterales y el tercer ventrículo aumentan progresivamente de tamaño con la duración de la enfermedad. Los cambios asociados con los síntomas negativos también se relacionan con la pérdida de volumen en el lóbulo temporal superior, el lóbulo temporal medial y el tálamo.
La alteración de la función ejecutiva se ha relacionado con anormalidades estructurales en el estriado, tálamo, cerebelo, giro cingulado anterior, hipocampo, lóbulo temporal medial, lóbulo frontal medial y corteza parietal posterior. Se concluye que la disfunción cerebral en pacientes esquizofrénicos se debe a una alteración en una serie de redes cerebrales en lugar de una única región.
Redes Cerebrales y Fisiopatología
El tálamo es la estación de relevo central que transmite información hacia y desde la corteza cerebral. El circuito primario responsable de los síntomas psicóticos se forma entre el tálamo, la corteza cerebral y el estriado asociativo. Cambios en cualquiera de estas regiones pueden afectar toda la red. Muchas más vías están involucradas directa o indirectamente con este circuito, como la amígdala y el hipocampo, responsables de la percepción y la regulación emocional. La disfunción del tálamo y la corteza cerebral afecta en gran medida el estriado y los receptores D2, causando alucinaciones y síntomas delirantes.
Neurobiología del Inicio y la Progresión
Un metaanálisis de pacientes esquizofrénicos sin medicación encontró una disminución del volumen intracraneal tanto en la esquizofrenia crónica como en la de inicio reciente. Esto sugiere que los pacientes comienzan a tener anormalidades en el volumen cerebral en la adolescencia temprana con el primer episodio, que continúan en mayor medida después del inicio de la enfermedad. Sin embargo, los cambios en la materia gris parecen ser más significativos después del inicio de la psicosis y muestran una relación directa con el uso de medicación y la recaída psicótica. En el primer episodio, hay evidencia de cambios en la materia blanca y gris a diferentes ritmos.
La esquizofrenia de inicio tardío se asocia con un mayor índice ventrículo-cerebro, anormalidades estructurales en las áreas frontal, subcortical y temporal, junto con desmielinización de la materia blanca. Interesantemente, la esquizofrenia de inicio tardío presenta un conjunto heterogéneo de síntomas, desde delirios y alucinaciones hasta deterioro cognitivo asociado con declives de memoria y disfunción ejecutiva, en comparación con la de inicio temprano.
La recaída en la esquizofrenia es multifactorial, involucrando factores genéticos, biológicos y ambientales. Puede ser idiopática o secundaria a la falta de adherencia a la medicación o al abuso de sustancias.
Deterioro Cognitivo y Función Cerebral
Los síntomas negativos junto con la disfunción cognitiva son la razón principal de la discapacidad funcional en la esquizofrenia. Aunque hay síntomas superpuestos, no todos los pacientes exhiben síntomas idénticos, lo que sugiere la existencia de subtipos. Se observa un deterioro evidente en la memoria de trabajo, memoria verbal, aprendizaje, funciones ejecutivas, atención, velocidad de procesamiento y discapacidad intelectual general en comparación con individuos no afectados.
Algunas teorías postulan que estas disfunciones cognitivas se deben a un deterioro en la conectividad entre las cortezas y las entradas de neurotransmisores. La función ejecutiva es un proceso multifacético que involucra diversas áreas cerebrales trabajando juntas. Estudios han demostrado disfunción de la corteza prefrontal y puntuaciones bajas en conceptualización, planificación, flexibilidad cognitiva, fluidez verbal y resolución de problemas complejos.
Los pacientes con esquizofrenia exhiben distorsión de la realidad, desorganización y pobreza psicomotora, fuertemente correlacionados con el deterioro ocupacional y social. En cuanto a la atención (sostenida, selectiva, alternante, dividida), los pacientes puntúan más bajo en pruebas como el Stroop, posiblemente debido a su incapacidad para enfocar y filtrar selectivamente. La memoria de trabajo, que recopila información, la codifica y la aplica, también muestra déficits severos en áreas fonológicas, visoespaciales y ejecutivas centrales. Aún no está claro si esta disfunción se debe a una región cerebral específica o a la incapacidad para sincronizar el sistema de redes complejas.
La neuropsicología subyacente a los síntomas positivos y negativos es compleja. Los síntomas negativos demuestran una falta de iniciación de emociones que causa aislamiento, mientras que los positivos se deben a sistemas de monitoreo interno anormales para el pensamiento y las acciones voluntarias. La corteza prefrontal, los ganglios basales y el hipocampo son las principales regiones cerebrales involucradas en la neuropsicología de estos síntomas.
Enfoques Farmacológicos
El manejo farmacológico de la esquizofrenia se basa principalmente en el bloqueo de los receptores D2 de dopamina en la vía mesolímbica. Los antipsicóticos de primera generación (APG) bloquean predominantemente los receptores D2 y son efectivos para los síntomas positivos, pero no para los negativos. Sus efectos secundarios más comunes son los síntomas extrapiramidales, asociados con el antagonismo de los receptores D2 en la vía nigroestriatal.
Los antipsicóticos de segunda generación (ASG) se desarrollaron para manejar tanto los síntomas positivos como negativos. Además de antagonizar los receptores D2, también antagonizan los receptores de serotonina 5HT, causando menos síntomas extrapiramidales. Sin embargo, presentan limitaciones en cuanto a efectos secundarios metabólicos (síndrome metabólico) e hipotensión. La clozapina se reserva para casos resistentes al tratamiento pero tiene efectos adversos graves como agranulocitosis.
El efecto de los ASG sobre los síntomas negativos es objeto de debate en ensayos clínicos. Aunque tienen más ventajas que los APG para estos síntomas, no son la solución definitiva. Se están investigando nuevos fármacos que modulan simultáneamente la neurotransmisión de serotonina, dopamina y glutamato, como el lumateperone, con menos efectos adversos debido a una menor interacción con otros receptores. Otro fármaco en investigación, SEP-363856, actúa sobre el receptor TAAR1 y 5-HT1A, mostrando una disminución significativa de los síntomas psicóticos con un perfil de efectos secundarios potencialmente más favorable, aunque se necesitan ensayos más largos y amplios.
En resumen, la esquizofrenia es una condición con profundas raíces en el cerebro, influenciada por una compleja interacción de factores genéticos, desregulaciones químicas y cambios estructurales. La investigación continua en neurociencia es clave para desentrañar completamente sus mecanismos y desarrollar tratamientos más efectivos y específicos.
Preguntas Frecuentes sobre las Causas Neurológicas
¿Es la esquizofrenia puramente genética?
No, aunque la genética juega un papel significativo con múltiples genes implicados, la esquizofrenia es multifactorial. Factores ambientales y cambios en la química y estructura cerebral también contribuyen a su desarrollo.
¿Qué neurotransmisores son más importantes en la esquizofrenia?
La dopamina, particularmente la disfunción subcortical, es considerada clave para los síntomas psicóticos. El glutamato y el GABA también están implicados, y la hipofunción de los receptores NMDA (relacionados con el glutamato) podría contribuir a la patogénesis.
¿Los cambios en la estructura cerebral son reversibles?
La información proporcionada no indica que los cambios estructurales como la pérdida de materia gris o el aumento ventricular sean reversibles. Estos cambios se observan con la progresión de la enfermedad, aunque el tratamiento temprano puede ayudar a controlar los síntomas y mejorar el pronóstico a largo plazo.
¿La esquizofrenia afecta solo a una parte específica del cerebro?
No, la investigación sugiere que la disfunción en la esquizofrenia se debe a problemas en una red de áreas cerebrales interconectadas, incluyendo la corteza prefrontal, lóbulos temporales, estriado, tálamo, hipocampo y cerebelo, en lugar de una única región.
¿Cómo actúan los medicamentos antipsicóticos a nivel neurológico?
La mayoría de los antipsicóticos actúan principalmente bloqueando los receptores de dopamina D2 en el cerebro. Los antipsicóticos de segunda generación también actúan sobre los receptores de serotonina. Se están desarrollando nuevos fármacos que modulan otros sistemas de neurotransmisores como el glutamato.
Comparativa: Síntomas Positivos vs. Negativos
La esquizofrenia se caracteriza por una amplia gama de síntomas que se clasifican típicamente en positivos y negativos. Comprender esta distinción es fundamental para entender cómo la enfermedad afecta el funcionamiento de un individuo, aunque ambos tipos de síntomas están relacionados con la disfunción de las redes cerebrales y los neurotransmisores.
| Síntomas Positivos | Síntomas Negativos |
|---|---|
| Reflejan la presencia de ideas, percepciones o acciones exageradas o distorsionadas que no están presentes en la realidad. | Reflejan la ausencia o disminución de funciones mentales o comportamientos normales. |
| Delirios (creencias falsas y fijas, ej., ser perseguido o tener habilidades especiales). | Afecto aplanado (reducción en la expresión de emociones). |
| Alucinaciones (percepciones sensoriales falsas, ej., escuchar voces o ver cosas que no existen). | Aislamiento social (retraimiento de interacciones sociales). |
| Lenguaje y pensamiento desorganizados (dificultad para organizar ideas, respuestas incoherentes, "ensalada de palabras"). | Anhedonia (incapacidad para experimentar placer). |
| Comportamiento motor extremadamente desorganizado o inusual (agitación, posturas extrañas, catatonia). | Apatía (falta de motivación o interés en actividades diarias). |
| Relacionados principalmente con la disfunción de la dopamina subcortical en el estriado. | Relacionados con la disfunción en áreas como el lóbulo temporal superior, el lóbulo temporal medial y el tálamo, y también vinculados a la disfunción de redes complejas y neurotransmisores como el glutamato y el GABA. |
Mientras que los síntomas positivos a menudo responden mejor a la medicación antipsicótica tradicional que actúa sobre la dopamina, los síntomas negativos y cognitivos representan un desafío terapéutico mayor y están más estrechamente relacionados con el deterioro funcional a largo plazo. La investigación actual busca comprender mejor las bases neurológicas específicas de cada tipo de síntoma para desarrollar tratamientos más dirigidos.
Si quieres conocer otros artículos parecidos a Esquizofrenia: Las Raíces en el Cerebro puedes visitar la categoría Neurociencia.