La psicosis es un estado mental caracterizado por una pérdida de contacto con la realidad, manifestándose a menudo como alucinaciones y delirios. Durante un episodio psicótico, los pensamientos y percepciones de una persona se distorsionan, dificultando la distinción entre lo real y lo irreal. Si bien las causas fundamentales de la psicosis son complejas y multifactoriales, la neurociencia moderna está desentrañando los intrincados mecanismos cerebrales que subyacen a estos síntomas.
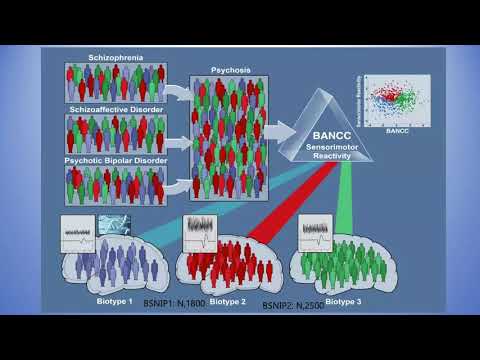
La investigación reciente, incluyendo un estudio liderado por Stanford Medicine, apunta a disfunciones clave en sistemas cerebrales específicos. En esencia, se ha identificado un fallo en un 'filtro' que dirige la atención hacia eventos externos e internos importantes, y en un 'predictor' compuesto por vías que anticipan recompensas. La alteración de estos sistemas fundamentales parece dificultar la capacidad del cerebro para determinar qué es real, culminando en las manifestaciones sintomáticas de la psicosis.

Sistemas Cerebrales Clave en la Disfunción Psicótica
El estudio de Stanford Medicine, basado en datos de resonancia magnética funcional (fMRI) de niños, adolescentes y adultos jóvenes con psicosis, ha proporcionado evidencia sólida para confirmar teorías existentes sobre cómo ocurren las rupturas con la realidad. Los hallazgos son consistentes tanto en individuos con el síndrome de deleción 22q11.2, una condición genética rara con un alto riesgo de psicosis, como en aquellos con psicosis de origen desconocido.
Los dos sistemas identificados como principales contribuyentes a la psicosis son:
1. El Sistema de Filtrado (Red de Saliencia): Normalmente, esta red neuronal opera de manera subconsciente para dirigir selectivamente nuestra atención hacia pensamientos internos y eventos externos importantes. Nos ayuda a descartar pensamientos irracionales o eventos sin importancia y a centrarnos en lo que es real y significativo. Una parte clave de este sistema es la ínsula anterior.
2. El Sistema Predictor (Estriado Ventral): Esta región cerebral, junto con las vías asociadas impulsadas por dopamina, juega un papel crucial en la predicción de lo que será gratificante o importante. Ayuda a atribuir relevancia a estímulos y pensamientos.
En la psicosis, el mal funcionamiento de estos sistemas cognitivos de control permite que pensamientos que no están vinculados a la realidad capturen la atención, permitiendo que pensamientos intrusivos dominen y se experimenten como alucinaciones (percepciones sensoriales sin estímulo externo) o delirios (creencias falsas y fijas).
Es notable que este estudio identificó que las anomalías en las interacciones funcionales entre regiones dentro de estos sistemas cerebrales pueden ser evidentes desde edades tempranas, incluso a los 7 u 8 años, mucho antes del inicio típico de la esquizofrenia en la adolescencia o adultez temprana. Esto sugiere la posibilidad de intervenciones tempranas dirigidas a estas áreas.
Más Allá del Filtro: Una Visión Neurobiológica Amplia
Si bien el fallo en los sistemas de filtrado y predicción es un hallazgo importante, la neurobiología de la psicosis es mucho más compleja e involucra una red de interacciones disfuncionales en el cerebro. La investigación ha explorado múltiples mecanismos, incluyendo desregulaciones de neurotransmisores, neuroinflamación, disfunción glial, alteraciones en el eje hipotalámico-pituitario-suprarrenal (HPA), la conexión intestino-cerebro, el estrés oxidativo y la disfunción mitocondrial.
Desequilibrios de Neurotransmisores
La Hipótesis de la Dopamina
Históricamente, la hipótesis de la dopamina ha sido la teoría dominante, postulando que los síntomas psicóticos se deben a la hiperactividad de las neuronas dopaminérgicas en la vía mesolímbica. Esta vía se proyecta desde el área tegmental ventral (ATV) hacia el núcleo accumbens y otras regiones como la amígdala, el hipocampo y el estriado. La disregulación de la dopamina en el estriado asociativo se ha vinculado a la atribución inapropiada de saliencia a ciertos estímulos, lo que se manifiesta en los delirios.
Esta hipótesis se basa en parte en el hecho de que los fármacos antipsicóticos, que son el tratamiento principal para la psicosis, actúan bloqueando los receptores de dopamina D2. Además, sustancias psicoestimulantes como las anfetaminas, la cocaína y el cannabis, que aumentan los niveles de dopamina, pueden inducir síntomas psicóticos en individuos sanos o empeorarlos en pacientes con esquizofrenia. El uso intensivo de cannabis, especialmente en la adolescencia temprana, se ha correlacionado con un mayor riesgo de desarrollar psicosis.
Sin embargo, la hipótesis de la dopamina por sí sola no explica completamente la complejidad de la psicosis, especialmente los síntomas negativos y los déficits cognitivos de la esquizofrenia. La investigación actual sugiere que la disfunción dopaminérgica es parte de una disfunción de red más amplia que involucra múltiples regiones cerebrales y neurotransmisores.
Glutamato y GABA
La hipótesis del glutamato propone que los síntomas psicóticos y los déficits cognitivos resultan de la hipofunción de los receptores NMDA (NMDAR) en interneuronas GABAérgicas en la corteza cerebral. Esto llevaría a una sobreactivación de la señalización del glutamato aguas abajo hacia el ATV, posiblemente aumentando la liberación de dopamina en el sistema mesolímbico. Existe un juego recíproco entre la dopamina y el glutamato; el aumento agudo de dopamina puede aumentar la señalización del glutamato, pero la hiperactividad dopaminérgica también puede ser una consecuencia de altos niveles de liberación de glutamato.
Los antagonistas de NMDAR, como la ketamina, son conocidos por inducir síntomas psicóticos, lo que apoya la hipótesis del glutamato. El desequilibrio entre las redes excitatorias (glutamato) e inhibitorias (GABA) contribuye a la disfunción de la red neural. Las anormalidades en la neurotransmisión GABA también están vinculadas a los efectos de la hipoactividad de NMDAR en las interneuronas GABA, lo que conduce a un desequilibrio E/I como posible mecanismo de aumento de la actividad dopaminérgica.
El aminoácido D-serina, un coagonista potente en el sitio de glicina del NMDAR, también ha sido objeto de gran interés. Se han propuesto anormalidades en los niveles de D-serina o en las enzimas que regulan su síntesis/catabolismo en la esquizofrenia.
Serotonina
La serotonina (5-HT) también está implicada en la fisiopatología de la psicosis. La hipótesis de la serotonina implica una activación excesiva de los receptores 5-HT2A, particularmente en neuronas glutamatérgicas. La regulación al alza de estos receptores puede llevar a un exceso de liberación de glutamato en la corteza. Muchos antipsicóticos atípicos bloquean tanto los receptores D2 de dopamina como los 5-HT2A de serotonina.

Los fármacos alucinógenos como la psilocibina y el LSD actúan como agonistas de los receptores 5-HT2A. Se ha propuesto que estos alucinógenos interactúan con un complejo de receptores 5-HT2AR/mGluR2, que integra la señalización de serotonina y glutamato para regular la 'filtración sensorial', cuya perturbación podría ocurrir en la psicosis.
Neuroinflamación y Células Gliales
Aunque el cerebro está protegido por la barrera hematoencefálica (BHE), existe una comunicación bidireccional significativa entre los sistemas nervioso e inmune. La inflamación crónica puede ser perjudicial y se considera un mecanismo subyacente en muchas neuropatologías.
Un estado inflamatorio caracterizado por concentraciones elevadas de citoquinas pro-inflamatorias (como IL-6, IL-8, TNF-α) es común en muchos trastornos psiquiátricos, y se ha observado que la neuroinflamación a menudo precede la aparición de los síntomas psicóticos, implicándola en la patogénesis.
Microglia
Las microglías son las células inmunes residentes del sistema nervioso central (SNC). En condiciones patológicas como la psicosis, pueden volverse crónicamente activas, liberando citoquinas pro-inflamatorias. Se ha informado un aumento de la activación microglial en pacientes con esquizofrenia, correlacionándose positivamente con la gravedad de los síntomas. La activación microglial crónica puede contribuir a la poda sináptica excesiva, la pérdida de volumen cortical y la disfunción celular en la corteza prefrontal (CPF), todas características de la psicosis. Las microglías activadas también pueden alterar la BHE. Se cree que los antipsicóticos pueden reducir la activación microglial.
Astrocitos
Los astrocitos son las células gliales más abundantes y desempeñan roles cruciales en la homeostasis del SNC. Regulan la nutrición neuronal, la formación y modulación de sinapsis, y el transporte de neurotransmisores como el glutamato y el GABA. Son fundamentales en el ciclo glutamato-glutamina, donde el glutamato liberado por las neuronas se convierte en glutamina en los astrocitos antes de regresar a las neuronas. Se ha observado una relación glutamina/glutamato elevada en el líquido cefalorraquídeo de pacientes con primer episodio psicótico y esquizofrenia no medicada.
Los astrocitos también influyen en la síntesis de D-serina. Pueden ser una fuente de especies reactivas de oxígeno y nitrógeno (ROS/RNS) en condiciones de estrés oxidativo y disfunción mitocondrial, lo que promueve la activación microglial y la neuroinflamación. A la inversa, el estrés oxidativo puede dañar los astrocitos. Además, los astrocitos son componentes clave de la unidad neurovascular de la BHE y pueden afectar su permeabilidad.
Oligodendrocitos
Los oligodendrocitos son las células que forman la mielina en el SNC, esencial para la comunicación neuronal eficiente. Se ha informado una densidad reducida de oligodendrocitos y mielinización anormal en ciertas regiones cerebrales (como la frontotemporal) en pacientes con esquizofrenia. La pérdida de mielina puede contribuir a retrasos en la velocidad de procesamiento. Estas células son susceptibles a la excitotoxicidad por glutamato y al estrés oxidativo. La pérdida de oligodendrocitos puede permitir la infiltración de citoquinas pro-inflamatorias y microglías reactivas. Existe una comunicación cruzada entre microglías, astrocitos y oligodendrocitos que influye en la mielinización.
| Tipo de Glía | Funciones Clave | Impacto Potencial en Psicosis |
|---|---|---|
| Microglia | Vigilancia inmune, respuesta inflamatoria, poda sináptica | Activación crónica, liberación de citoquinas pro-inflamatorias, poda sináptica excesiva, disrupción de la BHE, disfunción de CPF |
| Astrocitos | Homeostasis neuronal, transporte de neurotransmisores (glutamato, GABA), ciclo glutamato-glutamina, síntesis de D-serina, soporte de BHE, regulación de estrés oxidativo | Regulación alterada de glutamato/GABA, relación glutamina/glutamato elevada, síntesis reducida de D-serina, fuente/víctima de estrés oxidativo, disrupción de la BHE |
| Oligodendrocitos | Mielinización de axones | Densidad reducida, mielinización anormal, susceptible a excitotoxicidad y estrés oxidativo, contribuye a déficits cognitivos y alucinaciones |
Eje Hipotalámico-Pituitario-Suprarrenal (HPA)
El eje HPA es el sistema neuroendocrino responsable de la respuesta al estrés y el mantenimiento de la homeostasis. La disregulación de este eje se ha implicado en varios trastornos mentales, incluida la psicosis. Los factores estresantes psicosociales y el historial de trauma, especialmente en la infancia, se consideran factores de riesgo para el desarrollo de enfermedades psicóticas. Se hipotetiza que la exposición repetida a estresores lleva a una sensibilización al estrés y a la disregulación del eje HPA.
La hiperactividad del eje HPA se manifiesta a menudo como hipercortisolemia (niveles elevados de cortisol), lo cual se ha observado en pacientes psicóticos. El aumento de glucocorticoides como el cortisol puede influir directamente en la neurotransmisión dopaminérgica en la vía mesolímbica, potenciando la liberación de dopamina. Existe una comunicación bidireccional entre el eje HPA y la inflamación sistémica; la disrupción crónica de la homeostasis puede contribuir a los síntomas psicóticos a través de la neuroinflamación. Los antipsicóticos pueden suprimir la actividad del eje HPA, lo que podría ser otro mecanismo de su eficacia.
El Eje Intestino-Cerebro
El cerebro y el sistema gastrointestinal están en constante comunicación bidireccional a través del eje intestino-cerebro (GBA). La psicosis a menudo se asocia con inflamación gastrointestinal crónica, sugiriendo que la disfunción en la psicosis puede extenderse a cambios en el microbioma intestinal. El microbioma tiene funciones críticas en la regulación de la homeostasis del huésped y puede alterar directamente la mielinización, la neurotransmisión, la organización de la BHE, el eje HPA y las interacciones neurales-inmunes.
La investigación sugiere una alteración en la composición del microbioma intestinal en la psicosis. Ciertas bacterias o sus metabolitos pueden influir en los niveles de neurotransmisores (como glutamato, GABA, serotonina y dopamina) y en los procesos inflamatorios. La disrupción de la barrera epitelial intestinal ('intestino permeable') también es común en trastornos psicóticos y puede permitir que mediadores inflamatorios crucen la BHE. El microbioma intestinal también regula la maduración y función de las microglías y puede influir en la mielinización y la actividad del eje HPA. Curiosamente, los antipsicóticos pueden tener propiedades antibióticas y alterar la composición del microbioma intestinal, lo que podría influir en sus efectos terapéuticos y efectos secundarios metabólicos.
Estrés Oxidativo
El estrés oxidativo es un desequilibrio entre la producción de especies reactivas (ROS/RNS) y la capacidad del cuerpo para desintoxicarlas. El exceso de radicales libres puede causar daño molecular, disfunción celular y neurotoxicidad. Se cree que el estrés oxidativo interviene en las hipótesis de la psicosis relacionadas con la dopamina, el glutamato, el sistema inmune y la conectividad cerebral alterada.
Las ROS pueden bloquear los transportadores de dopamina (DATs), aumentando las concentraciones de dopamina en la hendidura sináptica. La autooxidación de niveles elevados de dopamina también es una fuente importante de estrés oxidativo. Además, el estrés oxidativo puede reducir la actividad de las enzimas antioxidantes. La excitotoxicidad inducida por glutamato, resultado de la hipofunción de NMDAR, también se asocia con la producción de ROS.

Existe una relación bidireccional entre el estrés oxidativo y la hipofunción de NMDAR. El estrés oxidativo puede dañar las interneuronas parvalbúmina (PVIs), que son particularmente susceptibles debido a su alta demanda metabólica. El daño a las PVIs contribuye al desequilibrio E/I y al aumento de dopamina. Las microglías y astrocitos reactivos también producen ROS, perpetuando un ciclo de inflamación. Aunque no se considera la única causa de la esquizofrenia, el estrés oxidativo puede contribuir al deterioro funcional.
Disfunción Mitocondrial
Las mitocondrias son cruciales para el metabolismo energético, el estrés oxidativo y la modulación de la actividad sináptica, produciendo la mayor parte del ATP celular. Se han informado déficits en la expresión de genes relacionados con la función mitocondrial y actividad reducida de complejos clave (I y IV) de la cadena de transporte de electrones en el cerebro de pacientes con esquizofrenia. La disfunción mitocondrial parece interactuar con la disfunción de neurotransmisores, el estrés oxidativo y la inflamación.
La dopamina puede inducir apoptosis a través de la disfunción mitocondrial. La afluencia excesiva de Ca2+ a través de NMDARs, observada en la esquizofrenia, puede causar sobrecarga de calcio en las mitocondrias, llevando a disfunción y activación de señales de muerte celular. Las mitocondrias pueden ser tanto una fuente de estrés oxidativo como víctimas de él. Las ROS producidas por las mitocondrias pueden aumentar la producción de citoquinas pro-inflamatorias, y a la inversa, las citoquinas elevadas pueden perturbar el sistema antioxidante mitocondrial.
Implicaciones para el Tratamiento y la Compasión
Comprender los mecanismos neurobiológicos de la psicosis tiene implicaciones significativas para el desarrollo de tratamientos y estrategias de prevención. La identificación de disfunciones tempranas en sistemas clave como el filtro y el predictor sugiere que las intervenciones dirigidas a estas áreas, posiblemente utilizando técnicas como la estimulación magnética transcraneal o el ultrasonido focalizado, podrían prevenir o retrasar el inicio de la psicosis en individuos de alto riesgo.
El conocimiento actual refuerza la idea de que la psicosis es una condición compleja que involucra múltiples sistemas cerebrales interconectados. Esto subraya la necesidad de enfoques de tratamiento multidisciplinarios, como la Atención Especializada Coordinada (CSC), que combina medicación antipsicótica con psicoterapia, apoyo familiar, servicios de empleo/educación y gestión de casos.
Finalmente, el avance en nuestra comprensión de la base neurobiológica de la psicosis también debe inspirar un cambio cultural hacia una mayor empatía y apoyo para quienes la experimentan. Reconocer que la psicosis es el resultado de disfunciones cerebrales complejas, y no una falla personal, es fundamental para reducir el estigma y fomentar un enfoque compasivo y solidario.
Preguntas Frecuentes sobre la Neurobiología de la Psicosis
¿Qué es la psicosis?
La psicosis es un conjunto de síntomas que afectan la mente y resultan en una pérdida de contacto con la realidad. Se caracteriza principalmente por delirios (creencias falsas) y alucinaciones (percepciones sensoriales sin estímulo externo).
¿Cuál es la causa principal de la psicosis?
No hay una única causa. La psicosis parece ser el resultado de una combinación compleja de factores genéticos, diferencias en el desarrollo cerebral, exposición a estresores o traumas, y disfunciones en múltiples sistemas neurobiológicos, incluyendo desequilibrios de neurotransmisores, neuroinflamación, y alteraciones en redes neuronales específicas.
¿Qué ocurre en el cerebro durante un episodio psicótico?
Durante la psicosis, sistemas cerebrales clave como el que filtra la información relevante y el que predice las recompensas pueden fallar. Esto dificulta la distinción entre lo real e irreal. También hay desequilibrios en neurotransmisores como la dopamina, el glutamato y la serotonina, así como procesos de neuroinflamación, estrés oxidativo y disfunción mitocondrial, que contribuyen a la alteración de la percepción y el pensamiento.
¿La psicosis está relacionada solo con la esquizofrenia?
No. Aunque la psicosis es una característica central de la esquizofrenia, también puede ocurrir como síntoma en otros trastornos mentales graves (como el trastorno bipolar o la depresión severa), en ciertas condiciones médicas (como enfermedades neurológicas en adultos mayores), o ser inducida por sustancias, medicamentos, o privación del sueño.
¿Se puede tratar la psicosis?
Sí, la psicosis se puede tratar. El tratamiento temprano es crucial para mejorar los resultados. Generalmente incluye medicación antipsicótica, que ayuda a manejar los síntomas. Además, se recomiendan enfoques terapéuticos integrales como la Atención Especializada Coordinada, que incluye psicoterapia, apoyo familiar y servicios de rehabilitación.
¿Los desequilibrios químicos son la única explicación de la psicosis?
Inicialmente, la hipótesis de la dopamina se centró en desequilibrios químicos. Sin embargo, la investigación actual muestra que la psicosis es mucho más compleja, involucrando no solo neurotransmisores, sino también procesos inflamatorios, la función de las células gliales, la respuesta al estrés, la conexión intestino-cerebro y la salud celular general (mitocondrias, estrés oxidativo). Es una disfunción compleja de redes cerebrales y sistemas biológicos interconectados.
Si quieres conocer otros artículos parecidos a Neurociencia de la Psicosis: El Cerebro Desconectado puedes visitar la categoría Neurociencia.

