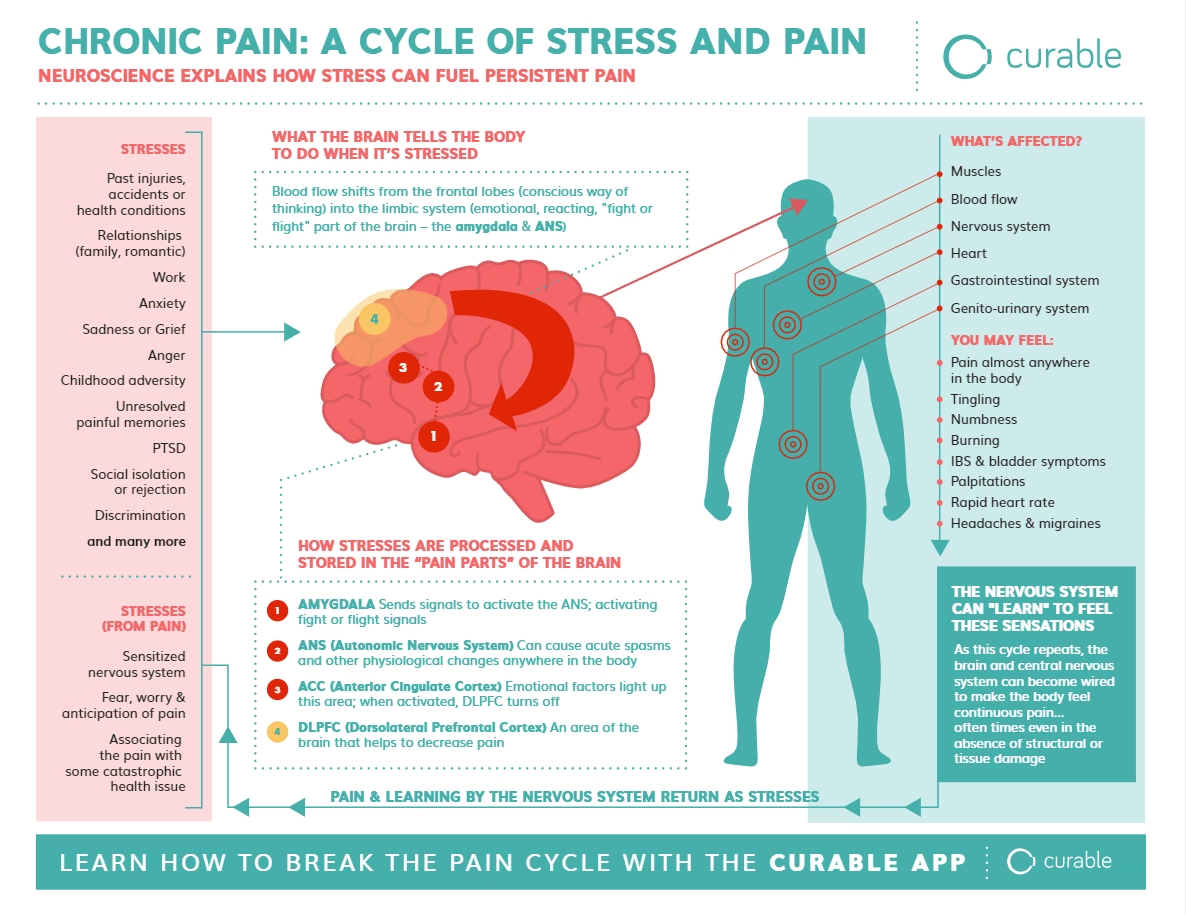
El dolor es una experiencia universal y compleja, mucho más que una simple sensación desagradable. Desde una perspectiva neurobiológica, el dolor es un fenómeno dinámico que involucra una intrincada red de células, vías nerviosas y regiones cerebrales que trabajan conjuntamente para detectar, transmitir, procesar y modular las señales relacionadas con el daño tisular o la amenaza al organismo. Comprender la neurobiología del dolor es fundamental no solo para desentrañar uno de los misterios del cuerpo humano, sino también para desarrollar estrategias más efectivas para su tratamiento, especialmente en el caso del dolor crónico que afecta a millones de personas en todo el mundo.

Esta área de estudio abarca desde los mecanismos moleculares y celulares en la periferia y la médula espinal hasta las complejas interacciones en el cerebro que dan lugar a la percepción consciente del dolor, su componente emocional y cognitivo, y las respuestas conductuales asociadas. Es un campo en constante evolución que busca tender puentes entre la investigación básica y su aplicación clínica.

- El Viaje de la Señal Dolorosa: Desde la Periferia hasta el Cerebro
- Neurotransmisores y Neuromoduladores Clave en el Dolor
- Dolor Agudo vs. Dolor Crónico: Un Cambio de Paradigma Neurobiológico
- Plasticidad Neuronal y Sensibilización
- El Papel de la Neuroinflamación
- Abordajes Terapéuticos Basados en la Neurobiología
- Preguntas Frecuentes sobre la Neurobiología del Dolor
El Viaje de la Señal Dolorosa: Desde la Periferia hasta el Cerebro
El proceso que lleva a la percepción del dolor, conocido técnicamente como nocicepción, comienza en los tejidos periféricos del cuerpo.
Nociceptores: Los Sensores del Daño
En la piel, músculos, articulaciones y órganos internos existen terminaciones nerviosas especializadas llamadas nociceptores. A diferencia de otros receptores sensoriales (que detectan tacto, temperatura suave, etc.), los nociceptores solo se activan cuando hay un estímulo potencialmente dañino o real. Pueden responder a diferentes tipos de estímulos:
- Mecánicos: Presión intensa, corte, aplastamiento.
- Térmicos: Temperaturas extremas (muy calientes o muy frías).
- Químicos: Sustancias liberadas por tejidos dañados o células inflamatorias (como bradiquinina, histamina, prostaglandinas, protones, ATP) o sustancias irritantes externas.
Estos nociceptores son las primeras sentinelas del sistema de alarma del cuerpo. Cuando se activan, generan una señal eléctrica (potencial de acción) que viaja a lo largo de la fibra nerviosa sensorial primaria.
Fibras Nerviosas: Las Vías de Conducción
Las señales de los nociceptores son transmitidas al sistema nervioso central a través de dos tipos principales de fibras nerviosas sensoriales primarias:
- Fibras Aδ (A-delta): Son mielinizadas, lo que les permite conducir impulsos rápidamente. Transmiten información sobre dolor agudo, punzante, bien localizado y de inicio rápido, como el que se siente inmediatamente después de golpearse un dedo.
- Fibras C: Son amielínicas (sin mielina), por lo que conducen impulsos más lentamente. Transmiten información sobre dolor sordo, quemante, mal localizado y de inicio más lento pero prolongado, característico del dolor asociado a la inflamación o el daño tisular persistente.
Es la combinación de señales de estas dos fibras lo que contribuye a la experiencia bifásica del dolor (un dolor inicial agudo seguido de un dolor más difuso).
La Médula Espinal: Primera Estación de Procesamiento
Las fibras sensoriales primarias entran en la médula espinal a través de las raíces dorsales y hacen sinapsis en las neuronas del asta dorsal. Aquí ocurre un procesamiento crucial de la señal.
- Sinapsis: Las fibras Aδ y C liberan neurotransmisores excitadores como el glutamato y la sustancia P, que activan las neuronas del asta dorsal.
- Modulación: La actividad en el asta dorsal no es una simple retransmisión. Está modulada por interneuronas locales (algunas excitadoras, otras inhibidoras) y por señales descendentes provenientes del cerebro. Esta modulación puede amplificar o atenuar la señal dolorosa. La "Teoría de la Compuerta" del Dolor, aunque simplificada, ilustra la idea de que la actividad de fibras no dolorosas (como las del tacto) puede "cerrar la compuerta" al dolor a nivel medular.
Desde el asta dorsal, las neuronas secundarias cruzan al lado opuesto de la médula espinal y ascienden hacia el cerebro a través de diferentes tractos, siendo el tracto espinotalámico el más conocido para el dolor y la temperatura.
El Cerebro: Donde la Nocicepción se Convierte en Dolor
Las vías ascendentes llevan la información nociceptiva a diversas regiones del cerebro, donde se integra para formar la experiencia multidimensional del dolor.
- Tálamo: Actúa como una estación de relevo principal, distribuyendo la información a varias áreas corticales y subcorticales. Tiene un papel en la conciencia inicial del dolor.
- Corteza Somatosensorial (S1 y S2): Involucrada en la discriminación sensorial del dolor: dónde está localizado, su intensidad y sus características (punzante, quemante, etc.).
- Sistema Límbico: Incluye estructuras como la amígdala, el hipocampo y la corteza cingulada anterior. Estas regiones son críticas para el componente afectivo-emocional del dolor (la desagradabilidad, el sufrimiento) y la memoria del dolor.
- Corteza Prefrontal: Contribuye al componente cognitivo del dolor: evaluación, significado, expectativas, y cómo el dolor afecta la atención y el comportamiento.
- Otras Áreas: La ínsula (integración interoceptiva), el cerebelo y diversas áreas del tronco encefálico también están implicadas.
La experiencia final del dolor no es solo la activación de estas áreas, sino la interacción compleja entre ellas, influenciada por el estado emocional, las experiencias pasadas, la cultura y las expectativas del individuo.
Neurotransmisores y Neuromoduladores Clave en el Dolor
La comunicación entre las neuronas en las vías del dolor depende de una variedad de sustancias químicas:
- Excitadores:
- Glutamato: Principal neurotransmisor excitador en el SNC, crucial en la transmisión rápida de señales en la médula espinal y el cerebro.
- Sustancia P: Un neuropéptido que modula la transmisión del dolor, especialmente en la médula espinal. Contribuye a la sensibilización central.
- Péptido relacionado con el gen de la calcitonina (CGRP): Importante en la vasodilatación neurogénica y la sensibilización.
- Inhibidores:
- GABA y Glicina: Neurotransmisores inhibidores que pueden frenar la transmisión de señales dolorosas, especialmente en la médula espinal.
- Opioides Endógenos (Endorfinas, Encefalinas, Dinorfinas): Producidos naturalmente por el cuerpo, actúan sobre receptores opioides en la médula espinal y el cerebro para inhibir la transmisión del dolor. Forman parte del sistema analgésico endógeno.
- Moduladores:
- Serotonina y Norepinefrina: Neurotransmisores monoaminérgicos que viajan por vías descendentes desde el tronco encefálico hasta la médula espinal, modulando la transmisión del dolor (pueden ser excitadores o inhibidores dependiendo del receptor).
- Endocannabinoides: Modulan la liberación de neurotransmisores y pueden tener efectos analgésicos.
- Citocinas y Quimiocinas: Moléculas liberadas por células inmunes y gliales durante la inflamación, que pueden sensibilizar nociceptores y neuronas del SNC.
Dolor Agudo vs. Dolor Crónico: Un Cambio de Paradigma Neurobiológico
Una distinción fundamental en la neurobiología del dolor es entre el dolor agudo y el dolor crónico. Aunque ambos comparten algunas vías iniciales, sus mecanismos subyacentes y su significado biológico son marcadamente diferentes.
El dolor agudo es generalmente una respuesta protectora a un daño tisular inminente o real. Es limitado en el tiempo y se resuelve cuando la lesión sana. Neurobiológicamente, implica la activación de las vías nociceptivas descritas anteriormente.
El dolor crónico, por otro lado, persiste mucho más allá del tiempo de curación esperado (generalmente definido como más de 3-6 meses) o existe en ausencia de un daño tisular continuo claro. A menudo, el dolor crónico no tiene un propósito biológico aparente y se considera una enfermedad en sí misma. Su neurobiología implica cambios profundos y persistentes en el sistema nervioso, conocidos colectivamente como plasticidad neuronal mal adaptativa.
| Característica | Dolor Agudo | Dolor Crónico |
|---|---|---|
| Duración | Corto (horas a días/semanas) | Prolongado (meses a años) |
| Propósito | Advertencia de daño, protector | Generalmente sin propósito protector aparente |
| Causa | Generalmente clara (lesión, infección, inflamación) | A menudo compleja, puede persistir después de la causa inicial; puede no haber daño tisular continuo |
| Mecanismos principales | Activación de vías nociceptivas | Plasticidad del sistema nervioso (sensibilización, cambios en la expresión génica, neuroinflamación, reorganización cerebral) |
| Respuesta al tratamiento | Suele responder bien a analgésicos convencionales | A menudo refractario a tratamientos convencionales; requiere enfoques multimodales |
| Impacto | Localizado, limitado | Amplio (físico, psicológico, social, económico) |
Plasticidad Neuronal y Sensibilización
El desarrollo del dolor crónico a menudo implica fenómenos de plasticidad neuronal. La plasticidad es la capacidad del sistema nervioso para cambiar su estructura y función en respuesta a la experiencia o a la lesión. En el contexto del dolor crónico, esta plasticidad puede llevar a:
- Sensibilización Periférica: Los nociceptores en la periferia se vuelven más sensibles a los estímulos, disminuyen su umbral de activación y aumentan su respuesta. Esto es común en la inflamación.
- Sensibilización Central: Quizás el mecanismo más importante en muchos síndromes de dolor crónico. Ocurre en el sistema nervioso central (médula espinal y cerebro). Las neuronas del asta dorsal se vuelven hiperexcitables, respondiendo de forma exagerada a las señales aferentes. Estímulos que antes no eran dolorosos (como un toque suave) pueden percibirse como dolorosos (alodinia), y estímulos dolorosos se perciben como mucho más intensos (hiperalgesia). Esto implica cambios a nivel sináptico (potenciación a largo plazo), en canales iónicos, y en la expresión génica de las neuronas.
- Reorganización de Circuitos: Las conexiones entre neuronas pueden modificarse, e incluso áreas cerebrales pueden reorganizarse funcionalmente, contribuyendo a la persistencia del dolor.
El Papel de la Neuroinflamación
La neuroinflamación, la respuesta inflamatoria dentro del sistema nervioso central, juega un papel crucial en el establecimiento y mantenimiento del dolor crónico. Células no neuronales como la microglia y los astrocitos, tradicionalmente vistas solo como células de soporte, se activan en respuesta a la lesión o la activación neuronal prolongada. Estas células activadas liberan una variedad de mediadores proinflamatorios (citocinas, quimiocinas) que pueden modular la actividad neuronal, amplificando las señales de dolor y contribuyendo a la sensibilización central. Dirigirse a la neuroinflamación es un área activa de investigación para nuevas terapias contra el dolor crónico.
Abordajes Terapéuticos Basados en la Neurobiología
Comprender los mecanismos neurobiológicos del dolor es esencial para desarrollar tratamientos efectivos. Los enfoques actuales y futuros buscan actuar sobre diferentes puntos de las vías del dolor:
- Actuar sobre Nociceptores: Anestésicos locales, capsaicina.
- Modular la Transmisión en la Médula Espinal: Opioides, algunos antidepresivos (inhibidores de la recaptación de serotonina y norepinefrina que potencian las vías descendentes inhibitorias), anticonvulsivos (que afectan canales iónicos).
- Influenciar el Procesamiento Cerebral: Terapias psicológicas (TCC, mindfulness) que actúan sobre los componentes cognitivos y emocionales del dolor; neuromodulación (estimulación cerebral profunda, estimulación de la corteza motora).
- Reducir la Sensibilización y la Neuroinflamación: Nuevos fármacos dirigidos a canales iónicos específicos, receptores de neurotransmisores, o mediadores inflamatorios liberados por células gliales.
Dado que el dolor crónico es a menudo un síndrome complejo con múltiples mecanismos implicados, los tratamientos más exitosos suelen ser multimodales, combinando farmacología, terapias físicas y psicológicas.
Preguntas Frecuentes sobre la Neurobiología del Dolor
- ¿Es el dolor completamente objetivo o subjetivo?
- La nocicepción (la señal de daño) es un proceso biológico objetivo, pero la experiencia del dolor es intrínsecamente subjetiva. Dos personas con la misma lesión pueden experimentar niveles de dolor muy diferentes debido a factores genéticos, psicológicos, sociales y culturales que modulan las vías cerebrales.
- ¿Puede el estrés o la ansiedad empeorar el dolor?
- Sí. El estrés, la ansiedad, la depresión y otros estados emocionales negativos activan regiones cerebrales (como la amígdala y la corteza prefrontal) que están interconectadas con las vías del dolor. Esto puede modular las señales descendentes a la médula espinal y aumentar la sensibilización central, amplificando la percepción del dolor.
- ¿Cómo funcionan los analgésicos más comunes a nivel neurobiológico?
- Varían: los AINE (antiinflamatorios no esteroideos) actúan principalmente en la periferia reduciendo la producción de mediadores inflamatorios. Los opioides actúan en la médula espinal y el cerebro inhibiendo la transmisión de señales dolorosas y activando sistemas analgésicos endógenos. Algunos antidepresivos y anticonvulsivos, utilizados para el dolor crónico, modulan la actividad neuronal y la sensibilización en el SNC.
- ¿Es el dolor fantasma real?
- Sí, es una experiencia de dolor muy real para la persona que lo sufre. Neurobiológicamente, se cree que el dolor fantasma se debe a cambios plásticos en el cerebro y la médula espinal que ocurrren después de la amputación, incluyendo reorganización cortical.
- ¿Por qué algunas personas desarrollan dolor crónico y otras no?
- La susceptibilidad al dolor crónico es compleja e influenciada por una combinación de factores genéticos, ambientales, psicológicos y sociales. La persistencia de la inflamación, la intensidad del dolor inicial, el manejo del estrés, la presencia de trastornos del estado de ánimo y la resiliencia individual juegan roles importantes.
En conclusión, la neurobiología del dolor revela un sistema fascinante y adaptable, diseñado para protegernos, pero que puede volverse disfuncional, llevando a condiciones de dolor crónico debilitantes. La investigación continua a nivel molecular, celular y de sistemas es crucial para desentrañar completamente estos mecanismos y pavear el camino hacia tratamientos más dirigidos y efectivos que puedan aliviar el sufrimiento asociado al dolor.
Si quieres conocer otros artículos parecidos a Neurobiología del Dolor: Un Vistazo Profundo puedes visitar la categoría Neurociencia.